
【题目】在25 ℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液。观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp(25 ℃)如下:
AgCl | AgI | Ag2S | |
Ksp(单位省略) | 1.8×10-10 | 1.5×10-16 | 6.3×10-50 |
下列叙述错误的是( )
A. 沉淀转化的实质就是沉淀溶解平衡的移动
B. 溶解度小的沉淀可以转化为溶解度更小的沉淀
C. AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D. 25 ℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】如图所示的实验装置可用来测定含两种元素的某种气体 X 的分子式。

在注射器A中装有240mL气体 X 慢慢通过不含空气并装有红热的氧化铜的玻璃 管B,使之完全反应,得到下面的实验结果:
实验前B管重20.32g,实验后B管重20.00g,B管中的黑色粉末变成红色粉末。在C管中收集到的无色液体是水;在注射器D中收集的气体是氮气。试回答下列问题:
(1)X气体是由______(填元素符号)元素组成的。
(2)若240mLX气体完全反应后,收集到的氮气质量是0.28g。根据实验时温度和压强计算 1molX气体的体积是24000mL,则X的摩尔质量是______。
(3)通过计算确定X的分子式为________。
(4)写出B中发生反应的化学方程式__________。(X在该条件下不发生分解反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用勒夏特列原理解释的事实是( )
A.棕红色的NO2加压后颜色先变深后变浅
B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深
C.黄绿色的氯水光照后颜色变浅
D.合成氨工业使用高压以提高氨的产量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于0.1 mol·L-1 Na2SO3溶液,正确的是( )
A. c(H+) +c(HSO3-) +2c(H2SO3) =c(OH-)
B. c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3)
C. c(Na+)+c(H+)=2c(SO32-)+2c(HSO3-)+c(OH-)
D. 升高温度,溶液pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沙罗特美是一种长效平喘药,其合成的部分路线如下:
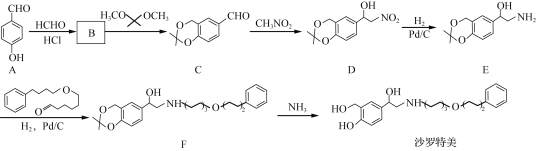
(1)F中的含氧官能团名称为____________(写两种)。
(2)C→D的反应类型为____________。
(3)B的分子式为C8H8O3,与(CH3)2C(OCH3)2发生取代反应得到物质C和CH3OH,写出B的结构简式:________。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式:__________。
①分子中含有苯环,且有一个手性碳原子,不能与FeCl3发生显色反应;
②能发生水解反应,水解产物之一是α氨基酸,另一含苯环的水解产物分子中只有3种不同化学环境的氢。
(5)请写出以 、(CH3)2C(OCH3)2、CH3NO2为原料制备
、(CH3)2C(OCH3)2、CH3NO2为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干) _____。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干) _____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组进行如下实验:
Ⅰ.探究反应速率的影响因素 设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol·L - 1 H2C2O4溶液、0.010 mol·L -1KMnO4 溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽

(1)若上述实验②、③是探究浓度对化学反应速率的影响,则 a 为______________;乙是实验需要测量的物理量,则表格中“乙”应 填写__________________。
Ⅱ.测定 H2C2O4·xH2O 中 x 值 已知:M(H2C2O4)=90 g·mol-1 ① 称取 1.260 g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液; ② 取 25.00 mL 待测液放入锥形瓶中,再加入适量的稀 H2SO4; ③ 用浓度为 0.05 000 mol·L -1 的 KMnO4 标准溶液进行滴定。
反应原理为:5 H2C2O4 + 2 MnO4— + 6H+ = 10CO2↑+ 2Mn2+ + 8H2O
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是________(选填 a、b)。由图可知消耗 KMnO4 溶液体积为________ mL。

(3)滴定终点锥形瓶内现象为__________________________________________________。
(4)通过上述数据,求得 x=______________。
(5)下列操作会造成所测x偏大的是____________(填字母)。
A.滴定终点俯视读数
B.锥形瓶用待测溶液润洗
C.滴定前有气泡,滴定后没有气泡
D.配制100mL待测溶液时,有少量溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元索对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是

A. 原于半径:r(Y)>r(Z)>r(W)
B. 化合物N、乙烯使溴水褪色的原理相同
C. 含W元素的盐溶液可能显酸性、中性或碱性
D. Z与X、Y、W形成的化合物中,各元素均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32- )、c(HCO3)都减少,其方法是
A. .加入氢氧化钠固体 B. 加氯化钠固体 C. 通入二氧化碳气体 D. 加入氢氧化钡固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com