
【题目】下列转化通过一步反应就能完成的是( )
A.N2→NO2B.S→SO3
C.Fe→FeCl3D.MgO→Mg(OH)2
科目:高中化学 来源: 题型:
【题目】氮氧化物是大气主要污染物,可采用强氧化剂氧化脱除、热分解等方法处理氮氧化物。
Ⅰ.已知:

(1)写出反应1的离子方程式___________。
(2)在反应2中,NO2-的初始浓度为0.1mol·L-1,反应为NO2-+S2O82-+2OH-![]() NO3-+2SO42-+H2O。不同温度下,达到平衡时NO2-的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如下图所示。
NO3-+2SO42-+H2O。不同温度下,达到平衡时NO2-的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如下图所示。

①比较a、b点的反应速率:va逆_______vb正(填或“>”“<”或“=”)
②随着温度的升高,该反应的化学平衡常数K______(填“增大”、“不变”或“减小”)。
③已知90℃时,Kw=3.6×10-13,若b点对应的pH为12,则该温度下K=_____(保留一位小数)。
(3)工业电解硫酸钠和硫酸的混合液制备过硫酸钠(Na2S2O8),阳极的电极反应式为_______。
Ⅱ.N2O在金粉表面发生热分解:2N2O(g)=2N2(g)+O2(g) ΔH。
回答下列问题:
(4)已知:2NH3(g)+3N2O(g)=4N2(g)+3H2O(1) ΔH1
4NH3(g)+3O2(g)=2N2(g)+6H2O(1) ΔH2
ΔH=_____。(含ΔH1、ΔH2的代数式)
(5)某温度下,测得c(N2O)随时间t变化关系如图所示。
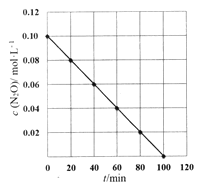
己知瞬时反应速率v与c(N2O)的关系为v=kcn(N2O)(k是反应速率常数),则k=________,n=_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,装置正确且能达到实验目的的是

A. 用图a所示装置验证H2在Cl2中燃烧的实验现象
B. 用图b所示装置从饱和食盐水中提取氯化钠
C. 用图c所示装置探究氧化性:KMnO4>Cl2>I2
D. 用图d所示装置分解MgCl2·6H2O获取MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向溶液M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断不正确的是(不计CO2溶解)
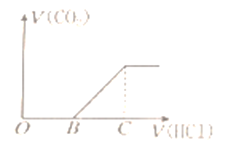
A. 若OB=0,则形成溶液的过程中所发生反应的离子方程式为OH―+CO2═HCO3―
B. 若OB=BC,则溶液M为Na2CO3溶液
C. 若OB>BC,则溶液M中大量存在的阴离子为CO32―和HCO3―
D. 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的资源,下图为海水利用的部分过程。下列有关说法正确的是

A. 由反应①可知:相同温度下,NaHCO3 的溶解度大于 Na2CO3
B. 反应②的离子方 程式为:Br2+SO2+2H2O=SO42-+2Br-+4H+
C. 可通过电解 MgCl2 溶液制得金属镁
D. 粗盐中含有的 Mg2+、SO4 2-等杂质离子,可通过依次加入 BaCl2溶液、NaOH 溶液、盐酸等试剂加以去除
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧氧化技术被广泛用于饮用水的处理,但也会产生易致癌的 BrO3-。
(1)取含 Br -的水样,向其中投加一定量的 H2O2 ,再经 O3氧化后,水中溴酸盐(BrO3-)的含量如图所示

①投加过氧化氢,其目的是___。
②未投加过氧化氢,臭氧投加量在 0~1.0 mg·L-1时,BrO3 -的浓度为 0 的可能原因是___ 。
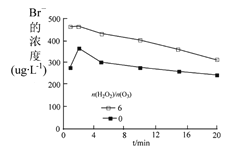
(2)科研小组在控制其他条件一定时,研究 n(H2O2)/n(O3) 对水样中 Br-浓度的影响,结果如图。在相同时刻,投加 H2O2 的反应中 Br-的浓度高于未投加 H2O2 的,其可能原因是反应过程中生成的HBrO 被 H2O2 还原所致,该反应的化学方程式为___ 。
(3)BrO3 -能被活性炭有效去除,其去除机理分为两步,第一步是___;第二步是 BrO3 -被活性炭还原为Br-。反应方程式(未配平)如下:
≡C+BrO3-→ BrO- + ≡CO2 ①
≡C+BrO-→ Br - + ≡CO2 ②
反应的总方程式为:2BrO3- + 3 ≡C = 2Br- + 3 ≡CO2。其中≡C 代表活性炭表面,≡CO2代表活性炭表面氧化物。则反应①与反应②中参加反应的≡C 物质的量之比为___ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合元素周期表回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界__________。
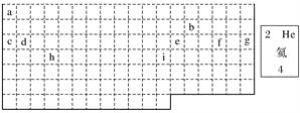
(2)表中所列元素,属于短周期元素的有________,属于主族元素的有________;g元素位于第________周期第________族;i元素位于第________周期第________族。
(3)元素f是第________周期第________族元素,请在下边方框中按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量。_____________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述错误的是
H++CH3COO-,下列叙述错误的是
A. 向溶液中加少量的CH3COONa固体,平衡逆向移动,c(CH3COO-)增大
B. 0.10mol/L的CH3COOH溶液中加少量水,平衡正向移动,导电性增强
C. 通入少量NH3气体,c(H+)减小、c(OH-)增加
D. 25℃时,加入少量浓醋酸,平衡正向移动,醋酸的电离程度减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法错误的是
A. 相同质量的CO与N2,所含分子数、原子数均相同
B. 56 g乙烯中所含共用电子对数目为12NA
C. 31 g白磷中所含共价键数目为NA
D. 14 g乙烯与丙烯的混合气体中所含氢原子数目为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com