
【题目】短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。下列说法正确的是( )
A. X的氢化物溶于水显酸性 B. Y原子的电子排布式为1s22s22p63s2
C. Z元素在周期表中的位置为第三周期第Ⅵ族 D. X和Z的最高价氧化物对应水化物都是弱酸
【答案】B
【解析】
短周期元素X、Y、Z的原子序数依次递增,Z原子最外层电子数是X原子内层电子数的3倍,则X只能有2个电子层,处于第二周期,X与Y、Z位于相邻周期,则Y、Z位于第三周期,故Z原子最外层电子数为6个电子,则Z为S;Z原子最外层电子数是Y原子最外层电子数的3倍,则Y原子最外层电子数为2,可推知Y为Mg;三原子的最外层电子数之和为13,则X的最外层电子数为![]() ,即X为氮元素。A.X的氢化物为氨气,氨气和水反应生成一水合氨,在水中电离生成按很离子合氢氧根离子,则溶液显碱性,故A错误;B.Y为Mg元素,原子核外有12个电子,核外电子排布式为
,即X为氮元素。A.X的氢化物为氨气,氨气和水反应生成一水合氨,在水中电离生成按很离子合氢氧根离子,则溶液显碱性,故A错误;B.Y为Mg元素,原子核外有12个电子,核外电子排布式为![]() ,所以B选项是正确的;C.Z为S,在周期表中的位置为第三周期第ⅥA族,故C错误;D.X和Z的最高价氧化物对应的水化物分别为硝酸、硫酸,都是强酸,故D错误.所以B选项是正确的.
,所以B选项是正确的;C.Z为S,在周期表中的位置为第三周期第ⅥA族,故C错误;D.X和Z的最高价氧化物对应的水化物分别为硝酸、硫酸,都是强酸,故D错误.所以B选项是正确的.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】密闭容器中有1mol NaHCO3和0.8mol Na2O2,加热充分反应后,容器内残留的固体
A. 0.5molNa2CO3和0.8mol Na2O2 B. 0.5molNa2CO3和1.6molNaOH
C. 0.8molNa2CO3和1molNaOH D. 1molNa2CO3和0.6molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】罗马大学Fulvio Cacace等人获得了极具理论研究意义的N4分子,N4分子结构如右图所示(与白磷P4相似)。已知断裂1 mol N—N键吸收167 kJ热量,生成 1 mol N≡N键放出 942 kJ 热量。由此判断下列说法正确的是( )
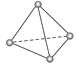
A. N4属于一种新型的化合物 B. N4与N2互为同分异构体
C. N4沸点比P4(白磷)高 D. 1 mol N4气体转变为N2将放出882 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】荧光棒的发光原理是利用过氧化氢氧化某草酸二酯产生能量传递给荧光物质发出荧光。该草酸二酯的结构简式如下图所示。下列有关该草酸二酯的说法不正确的是
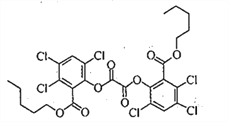
A. 分子中含有一种含氧官能团
B. 苯环上的一溴代物只有一种
C. 可以发生取代反应和加成反应
D. lmol草酸二酯与NaOH溶液反应最多消耗4mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾和碘的相关化合物在化工医药材料等领域有着广泛的应用。回答下列问题:
(1)基态K原子中,核外电子的空间运动状态共____种,占据最高能级的电子的电子云轮廓图形状为________。
(2)K和Cr属于同一周期,且核外最外层电子构型相同。第一电离能比较:K____(填“>”或“<”)Cr,金属键强度比较:K________(填“>”或“<")Cr.
(3)IO3-离子的立体构型的名称为_____,中心原子的杂化方式为________.
(4)HIO4的酸性强于HIO3,其原因为_________
(5)KIO3晶体是一种性能良好的非线性光学材料,晶胞如图所示。
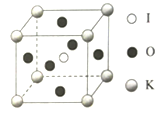
晶胞的棱长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,K与I间的最短距离为_______nm,与K紧邻的O的个数为______。阿伏加德罗常数的值为6.02×1023,列式计算晶体的密度为_________g/cm3.(不必计算结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 在常温、常压下,11.2 L N2含有的分子数为0.5NA
B. 标准状况下,22.4 L H2和O2的混合气体所含分子数为NA
C. 18 g H2O的物质的量是1mol
D. 标况下,1 mol SO2的体积是22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1mol·L-1KOH溶液滴定20mL0.1mol·L-1H2A溶液的滴定曲线如图所示(曲线上的数字为pH)。已知pKa=-lgKa,25℃时H2A的pKa1=1.85,pKa2=7.19。下列说法正确的是( )

A. a点所得溶液中:2c(H2A)+c(A2-)=0.1mol/L
B. b点所得溶液中:2c(H2A)+c(H+)=c(A2-)+c(OH-)
C. c点所得溶液中:c(K+)<3c(HA-)
D. d点所得溶液中A2-第一级水解平衡常数为10-6.81
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设某元素的原子核内的质子数为m,中子数为n,则下述论断正确的是( )
A. 不能由此确定该元素的相对原子质量
B. 这种元素的相对原子质量为(m+n)g
C. 碳原子质量为wg,此原子的质量为(m+n)wg
D. 核内中子的总质量小于质子的总质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com