
| �������� | ��ʼ������pH | ������ȫ��pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
���� �������ø��ֽⷴӦԭ������FeSO4��Na2CO3�Ƶ�FeCO3�����������ᷴӦ����������������������FeCO3 ʱҪ����Na2CO3�Լ��ԣ�ֻ�ܽ�Na2CO3��Һ�������뵽FeSO4��Һ�У������������Fe��OH��2������Ϊ�Ʊ����������������������뽫Na2CO3ϴ�Ӹɾ�����ȥ���溬��SO42-�IJ�����Һ��ͬʱ���������з�ֹ+2�������������������������Ҫ�ӷ�Ӧ���Һ�з������ʱ��ͨ������Ũ���ᾧ�ķ����õ���
��1������Na2CO3��Һ��FeSO4��Һ��Ӧ�Ʊ�FeCO3������Na2CO3��Һ���Ժ�ǿ�����ܻ�����Fe��OH��2������Ϊ��������Fe��OH��2�����������Na2CO3����FeSO4��Һ�У�Fe2+�ǹ����ģ�����FeSO4��ҺΪ���ԣ�Fe2+���׳�������ˣ�CO32-������Fe2+���Ϊ�������������Ӧ��Na2CO3��Һ�������뵽ʢ��FeSO4��Һ�ķ�Ӧ�����У�
��2���жϳ����Ƿ�ϴ���ķ�����ȡ���һ��ϴ�ӵ���Һ�������Һ���Ƿ����δϴ�Ӹɾ������ʣ�����ҪŪ������ϵ�������ʲô��Ȼ����ȥ�����������ӣ�������FeCO3���Ʊ�����Na2CO3��Һ��FeSO4��Һ�ķ�Ӧ���������������ܻ���Na2SO4���ʣ����Ӧ�ü������һ��ϴ����Һ���Ƿ���SO42-���������ת����SO42-�ļ��飻
��3����+2��FeԪ���ױ������е������������Ʊ�����������������Ӧ���������������Ӵ����������۵�Ŀ�ľ����������ᷴӦ����H2���γ�һ�������Ļ�������ȥ���������ۿ�ֱ�Ӽ��������������ᣬ��ӦҲ��������Ҫ�IJ�Ʒ�����������������������ʣ�
��4��������Һ��Ũ���γ������������ı�����Һ��Ҫ�õ������ܶ���������������壬�ɼ�����ˮ�Ҵ������Խ����������������ܽ�ȣ��Ӷ���ø���IJ�Ʒ��
��� �⣺��1������Na2CO3��Һ��FeSO4��Һ��Ӧ�Ʊ�FeCO3������Na2CO3��Һ���Ժ�ǿ�����ܻ�����Fe��OH��2�����������Na2CO3����FeSO4��Һ�У�Fe2+�ǹ����ģ�����FeSO4��ҺΪ���ԣ�Fe2+���׳�������ˣ�CO32-������Fe2+���Ϊ�������������Ϊ��������Fe��OH��2������Ӧ��Na2CO3��Һ�������뵽ʢ��FeSO4��Һ�ķ�Ӧ�����У��ʴ�Ϊ��c����������Fe��OH��2������
��2��Na2CO3���溬��SO42-�IJ�����Һ��ֻҪϴ��Һ����鲻��SO42-������֤��ϴ�Ӹɾ������������ȡ���һ��ϴ�ӵ���Һ��1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
�ʴ�Ϊ��ȡ���һ�ε�ϴ����Һ1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
��3����+2��FeԪ���ױ������е������������Ʊ�����������������Ӧ���������������Ӵ����������۵�Ŀ�ľ����������ᷴӦ����H2���γ�һ�������Ļ�������ȥ���������ۿ�ֱ�Ӽ��������������ᣬ��ӦҲ��������Ҫ�IJ�Ʒ�����������������������ʣ�
�ʴ�Ϊ����ֹ+2�۵���Ԫ�ر��������������������������۷�Ӧ��ȫ��
��4��������Һ��Ũ���γ������������ı�����Һ��Ҫ�õ������ܶ���������������壬�ɼ�����ˮ�Ҵ������Խ����������������ܽ�ȣ��Ӷ���ø���IJ�Ʒ��
�ʴ�Ϊ������������������ˮ�е��ܽ����������ھ���������
���� ���⿼����ѧ�������龳�����ʵ��Ʊ�ʵ���л�����ʵ�鼼�ܺͶԽ̲����ʵ��������Ǩ���������е����Ѷ�ƫ�������������ʺ�ʵ�鼼���ǽ���ؼ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | CH4 | B�� | C2H6 | C�� | C2H2 | D�� | C3H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
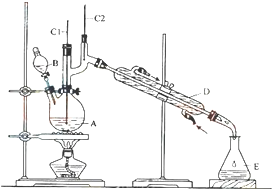 ����ȩ��һ�ֻ���ԭ�ϣ�ijʵ��С��������ͼװ�úϳ�����ȩ�������ķ�Ӧ���£�
����ȩ��һ�ֻ���ԭ�ϣ�ijʵ��С��������ͼװ�úϳ�����ȩ�������ķ�Ӧ���£�| �е�/0C | �ܶ�/��g•cm-3�� | ˮ���ܽ��� | |
| ������ | 117.2 | 0.8109 | �� |
| ����ȩ | 75.7 | 0.8017 | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com