
���� ��1��ͭ��Ũ�����ڼ��������·�Ӧ��������ͭ���������������ˮ������ֻ��Ũ������ܺ�ͭ��Ӧ�������ŷ�Ӧ�Ľ�������Ũ�ȱ�С��ϡ�����ͭ��Ӧ������������ʣ�ࣻ
��2���ӷ�Ӧ�����ۿ����ԣ�ʵ�ʿɲ����ԣ����������ԣ�������ȫ�Եȷ�����п��Ƿ������Աȼ��ҷ�Ӧ���̷�����֪���ף�Ũ����ֱ�Ӻ�ͭ��Ӧ�������SO2����Ⱦ�����������������Ҳ�࣬��ͬѧ��Ƶ��Ʊ����̣����ɵ���������ͭ�����������٣���Ӧ����������������Ⱦ�������ɣ�
��3��ͭ��ϡ�������ڼ��ȵ������²���ͨ���������Ӧ��������ͭ��ˮ��
��� �⣺��1���ڼ��������£�ͭ��Ũ���ᷴӦ��������ͭ���������������ˮ����Ӧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��ͭ�ڽ����˳�����������ĺ��棬����ϡ���ᷴӦ������ֻ��Ũ������ܺ�ͭ��Ӧ�������ŷ�Ӧ�Ľ�������Ũ�ȱ�С��ϡ�����ͭ��Ӧ��������ƿ�л��н϶������ʣ�࣬
�ʴ�Ϊ���ǣ����ŷ�Ӧ�Ľ�������Ũ�ȱ�С��ϡ�����ͭ��Ӧ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
��2���Ա�������Ʒ������ף�Cu+2H2SO4��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$SO2��+CuSO4+2H2O��
�ң�2Cu+O2 $\frac{\underline{\;\;��\;\;}}{\;}$2CuO��CuO+H2SO4=CuSO4+H2O�����Կ�����ȡ����������ͭ���ҷ������ĵ������٣����Ҳ�����û���ж����壬
�ʴ�Ϊ�����������٣���û����Ⱦ��SO2������
��3��ͭ��ϡ�������ڼ��ȵ������²���ͨ���������Ӧ��������ͭ��ˮ������ʽΪ2Cu+O2+2H2SO4$\frac{\underline{\;\;��\;\;}}{\;}$2CuSO4+2H2O��
�ʴ�Ϊ��2Cu+O2+2H2SO4$\frac{\underline{\;\;��\;\;}}{\;}$2CuSO4+2H2O��
���� ����ͨ�����÷�ͭ��ȡCuSO4����Ũ����Ļ�ѧ���ʺ���ɫ��ѧ�����ؿ�������ͭ�Ʊ��ķ������ۣ�ע��ʵ�鷽�����Ӧ������ȷ���������С����ý�Լ����ɫ��������Ŀ�Ѷ��еȣ�


 ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ħ���DZ�ʾ���������ĵ�λ | |
| B�� | Ħ���ǹ����߸�����������֮һ | |
| C�� | ��Ħ����ʾ���ʵ���ʱ��Ҫ�û�ѧʽָ���������� | |
| D�� | Ħ���������ʵ����ĵ�λ���������ӵ�������λ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �������� | ��ʼ������pH | ������ȫ��pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
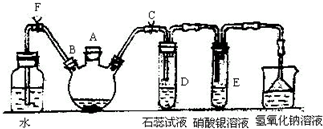 ʵ�����Ʊ��屽������ͼ��ʾ��װ�ã���д���пհף�
ʵ�����Ʊ��屽������ͼ��ʾ��װ�ã���д���пհף� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �� | �� | �� | �� | �� | �� |
| �� �� �� װ �� ͼ |  |  |  |  |  |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com