
| A. | 摩尔是表示物质质量的单位 | |
| B. | 摩尔是国际七个基本物理量之一 | |
| C. | 用摩尔表示物质的量时,要用化学式指明粒子种类 | |
| D. | 摩尔既是物质的量的单位,又是粒子的数量单位 |
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)2═Ca2++2OH- | B. | Al2(SO4)3═2Al3++3SO42- | ||
| C. | NH4Cl═NH3+H++OH- | D. | HNO3═H++NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH4 | B. | C2H6 | C. | C2H2 | D. | C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
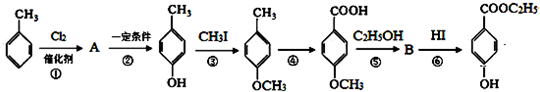
 .
.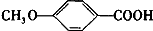 +C2H5OH$?_{△}^{浓硫酸}$
+C2H5OH$?_{△}^{浓硫酸}$ +H2O.
+H2O.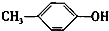 +CH2I→
+CH2I→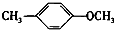 +HI.
+HI.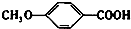 的同分异构体有多种,其中既含有酚羟基又含有酯基的同分异构体共有19种.
的同分异构体有多种,其中既含有酚羟基又含有酯基的同分异构体共有19种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉可长期放置在烧杯中 | |
| B. | 金属钠燃烧时不能用水灭火,应该用沙子灭火 | |
| C. | 氯水可以用无色透明的试剂瓶装保存 | |
| D. | 实验后剩余的钠不可放回原试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com