
【题目】(1)依据氧化还原反应2Ag+(ag)+Cu(s)==Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
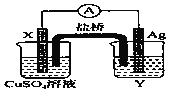
电极X的材料是_______;电解质溶液Y是_________________;银电极为电池的________极,发生的电极反应为______________________;X电极上发生的电极反应为______________________。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为氢氧燃料电池,
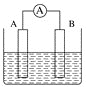
写出A电极反应式:___________________________________;写出B电极反应式:_______________________;写出该电池反应:__________。
【答案】铜(或Cu) AgNO3溶液 正 Ag++e-=Ag Cu-2e-=Cu2+ CH4+10OH--8e-=CO32-+7H2O 2O2+8e-+4H2O═8OH- CH4+2O2+2OH-═CO32-+3H2O
【解析】
(1)根据反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”分析,在反应中,Cu被氧化,失电子,应为原电池的负极,则Ag为正极,据此分析解答;
(2)甲烷燃料电池中通入CH4的电极为负极,通入氧气的电极为正极,据此分析解答。
(1)根据反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”分析,在反应中,Cu被氧化,失电子,应为原电池的负极,电极反应为Cu-2e-=Cu2+,选择硫酸铜为电解质,则Ag为正极,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,应该选用AgNO3为电解质溶液,故答案为:铜(或Cu);AgNO3溶液;正;Ag++e-=Ag;Cu-2e-=Cu2+;
(2)通入CH4的一极为负极,发生氧化反应,在碱性溶液中生成碳酸盐,电极反应为:CH4+10OH--8e-=CO32- +7H2O,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为:2O2+8e-+4H2O═8OH-,电池的总反应为CH4+2O2+2OH-═CO32- +3H2O,故答案为:CH4+10OH--8e-=CO32-+7H2O;2O2+8e-+4H2O═8OH-;CH4+2O2+2OH-═CO32-+3H2O。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】某同学结合所学知识探究Na2O2与H2能否反应,设计装置如下,下列说法正确的是

A. 装置A气密性的检查方法,直接向长颈漏斗中加水,当漏斗中液面高于试管中液面且高度不变说明气密性良好
B. 装置B中盛放硅胶,目的是除去A中挥发出来的少量水蒸气
C. 装置C加热前,用试管在干燥管管口处收集气体点燃,通过声音判断气体纯度
D. 装置A也可直接用于Cu与浓硫酸反应制取SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组顺序的排列不正确的是( )
A. 熔点:金刚石>干冰 B. 稳定性:SiH4>H2S
C. 碱性:KOH>Al(OH)3 D. 离子半径:O2->Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,B是地壳中含量最高的金属元素,C单质的晶体是良好的半导体材料,D的最外层电子数与内层电子数之比为3:5。
(1)C的原子结构示意图为______,D在元素周期表中的位置______。
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为________;A单质在E单质中燃烧生成化合物乙,用电子式表示乙的形成过程__________________。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为________________。
(4)E元素的非金属性强于D元素,用原子结构解释原因:同周期元素随着原子序数的递增,______________________________,非金属性增强。
(5)工业上将干燥的E单质通入D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关“绿色奥运”,下列环保建议中,你认为不能采纳的是
A.提倡生活垃圾分类收集
B.用天然气代替汽油和柴油作发动机燃料
C.禁止未经处理的工业废水和生活污水的任意排放
D.使用添加剂抑制水中所有动植物的生长
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用系统命法写出下列物质名称:
(1)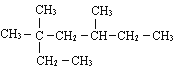 _______________;
_______________;
(2)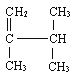 _______________;
_______________;
(3)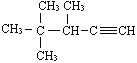 的系统名称为_______________;
的系统名称为_______________;
(4)键线式![]() 表示的分子式_______________;名称是_______________。
表示的分子式_______________;名称是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确是
A.溴元素被称为“海洋元素”
B.I、Mg、Br、U元素属于海水中的微量元素
C.碘是人体必须微量元素,所以要多吃富含高碘酸的食物
D.Li、Cl、Na、K元素属于海水中的常量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的结构简式为![]() ,判断下列说法中不正确的是
,判断下列说法中不正确的是
A. 它可以使酸性KMnO4溶液褪色
B. 它可以使溴水褪色
C. 它可与Cl2发生取代反应
D. 1mol该有机物燃烧消耗氧气为15mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com