
【题目】(1)磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)═6CaO(s)+P4(s)+10CO(g)△H1=+3359.26 kJmol﹣1
CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣89.61 kJmol﹣1
写出白磷(P4)由Ca3(PO4)2、焦炭和SiO2在一定条件下反应的热化学方程式为:_____。
(2)电子工业中清洗硅片上的SiO2(s)的反应为SiO2(s)+4HF(g)═SiF4(g)+2H2O(g)△H(298.15 K)=﹣94.0 kJmol﹣1△S(298.15 K)=﹣75.8 Jmol﹣1K﹣1,设△H和△S不随温度而变化,此反应自发进行的温度是_____
【答案】2Ca3(PO4)2(s)+6SiO2(s)+10C(s)═6CaSiO3(s)+P4(s)+10CO(g)△H=+2821.6kJmol﹣1 T<1240K。
【解析】
(1)根据盖斯定律①+②×6计算;
(2)反应自发进行的条件是△H﹣T△S=0计算临界温度。
(1)Ca3(PO4)2、焦炭和SiO2在一定条件下反应生成白磷(P4)的化学方程式为2Ca3(PO4)2(s)+6SiO2(s)+10C(s)═6CaSiO3(s)+P4(s)+10CO(g),
①2Ca3(PO4)2(s)+10C(s)═6CaO(s)+P4(s)+10CO(g)△H1=+3359.26 kJmol﹣1
②CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣89.61 kJmol﹣1
根据盖斯定律①+②×6计算2Ca3(PO4)2(s)+6SiO2(s)+10C(s)═6CaSiO3(s)+P4(s)+10CO(g)的焓变△H=+3359.26 kJ/mol+(﹣89.61 kJmol)×6=+2821.6kJ/mol,
故答案为:2Ca3(PO4)2(s)+6SiO2(s)+10C(s)═6CaSiO3(s)+P4(s)+10CO(g)△H=+2821.6kJmol﹣1
(2)反应自发进行的条件是△H﹣T△S<0,△S<0,则反应自发进行时T![]() 1240K,
1240K,
故答案为:T<1240K。


科目:高中化学 来源: 题型:
【题目】室温下,某二元碱X(OH)2水溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示,下列说法错误的是

A. Kb2的数量级为10-8
B. X(OH)NO3水溶液显碱性
C. 等物质的量的X(NO3)2和X(OH)NO3混合溶液中 c(X2+)>c[X(OH)+]
D. 在X(OH)NO3水溶液中,c[X(OH)2]+c(OH-)= c(X2+)+ c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T ℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示。下列说法中不正确的是( )

A.T ℃时,在Y点和Z点,Ag2CrO4的Ksp相等
B.a=![]() ×10-5
×10-5
C.T ℃时,Ag2CrO4的Ksp为1×10-11
D.向饱和Ag2CrO4溶液中加入固体K2CrO4不能使溶液由Y点变为X点图中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温、恒压下,在一个容积可变的容器中发生如下反应:A(g)+B(g)C(g)
(1)若开始时放入1mol A和1mol B,达到平衡后,生成a mol C,这时A的物质的量为_____ mol。
(2)若开始时放入3mol A和3mol B,达到平衡后,生成C的物质的量为_____mol。
(3)若开始时放入x mol A、2mol B和1mol C,达到平衡后,A和C的物质的量分别为y mol和3a mol,则x=_____,y=_____。
(4)若在(3)的平衡混合物中再加入3mol C,待再次达到平衡后,C的物质的量分数是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应CO+H2O(g)CO2+H2,回答下列问题:
(1)830 K时,若起始时c(CO)=2 molL﹣1,c(H2O)=3 molL﹣1,平衡时CO的转化率为60%,水蒸气的转化率为_____;平衡常数K的值为_____。
(2)830 K时,若只将起始时c(H2O)改为6 molL﹣1,则水蒸气的转化率为_____。
(3)若830 K时,某时刻混合体系中各气体的浓度为c(CO2)=0.4 molL﹣1、c(CO)=0.6 molL﹣1、c(H2O)=3 molL﹣1,c(H2)=2 molL﹣1请判定该体系中反应进行的方向:_____ (填“正向进行”“逆向进行”或“达到平衡”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数。可供选用的试剂有:浓H2SO4、浓硝酸、6 mol·l-1NaOH溶液。
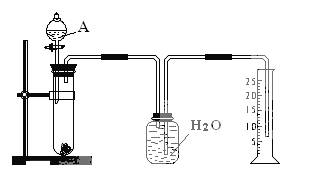
请填写下列空白:
(1)有关实验操作:a、往试管中放入适量的铝合金样品;b、从分液漏斗往试管中加入过量的A溶液;c、检查装置的气密性;d、测定收集到的水的体积。
正确的操作顺序为_________________________________________。
(2)A溶液可选用________________________________________
(3)若实验中测得样品的质量为W g ,氢气的体积为a L(标准状况),则样品中Al的质量分数为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象![]() 见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系
见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系![]() 。
。
实验步骤 | 实验现象 |
| A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| B.有气体产生,溶液变成浅红色 |
| C.剧烈反应,迅速产生大量无色气体 |
| D.反应不十分剧烈,产生无色气体 |
| E.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的: ______ 。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制![]() 溶液等.仪器:① ______ ,② ______ ,③ ______ ,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等。
溶液等.仪器:① ______ ,② ______ ,③ ______ ,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等。
(3)实验内容:![]() 填写与实验步骤对应的实验现象的编号和离子方程式
填写与实验步骤对应的实验现象的编号和离子方程式![]() _______________________
_______________________
实验内容 | 实验现象 | 离子方程式 |
1 | ||
2 | ||
3 | ||
4 | ||
5 |
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的相对强弱,请你设计实验![]() 实验用品自选,不要求写化学方程式
实验用品自选,不要求写化学方程式![]() : ______ 。
: ______ 。
(5)实验结论: ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯碳酸锰(MnCO3)广泛应用于电子行业,制造高性能磁性材料。工业利用含锰废水(主要含Mn2+、![]() 、H+、Fe2+、Al3+、Cu2+)制备碳酸锰、回收硫酸铵的工艺流程如下:
、H+、Fe2+、Al3+、Cu2+)制备碳酸锰、回收硫酸铵的工艺流程如下:

已知某些物质完全沉淀的pH值如表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 | Mn(OH)2 | CuS | MnS | MnCO3 |
沉淀完全时的pH | 3.7 | 5.2 | 6.4 | 9.8 | ≥0 | ≥7 | ≥7 |
回答下列问题:
(1)试剂X是___________ (填标号)。
a.Cl2 b.MnO2 c.浓HNO3 d.H2O2
(2)“滤渣1”中主要成分的化学式为__________。
(3)“除重金属”时发生反应的离子方程式是______;反应中使用(NH4)2S而不使用Na2S的原因是________。
(4)“50℃碳化”得到高纯碳酸锰,反应的离子方程式为_____,反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4,加入稍过量的NH4HCO3的目的是______使MnCO3沉淀完全,溶液的pH不能过低的原因是_____。
(5)由 MnCO3可制得重要的催化剂MnO2,2MnCO3+O2=2MnO2+2CO2。现在空气中加热460.0g的MnCO3,得到332.0g产品,若产品中杂质只有MnO,则该产品MnO2的质量分数是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一体积可变的容器中进行。下列条件的改变对其化学反应速率几乎没有影响的是:①增加C的用量;②将容器体积缩小一半;③保持容器体积不变,充入氮气使容器内压强增大;④保持压强不变,充入氮气使容器的体积变大
CO(g)+H2(g)在一体积可变的容器中进行。下列条件的改变对其化学反应速率几乎没有影响的是:①增加C的用量;②将容器体积缩小一半;③保持容器体积不变,充入氮气使容器内压强增大;④保持压强不变,充入氮气使容器的体积变大
A. ②④ B. ①③ C. ③④ D. ①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com