
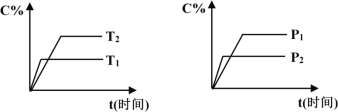
【题目】可逆反应mA(固)+nB(气)![]() pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
A. 达到平衡后,使用催化剂,C%将增大
B. 达到平衡后,若升高温度、化学平衡向逆反应方向移动
C. 方程式中n>p+q
D. 达到平衡后,增加A的量有利于化学平衡向正反应方向移动
【答案】B
【解析】
可逆反应,当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短。由图象(1)可知T1>T2,温度越高,平衡时C的体积分数φ(C)越小,故此反应的正反应为放热反应;
当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短。由图(2)可知P2>P1,压强越大,平衡时C的体积分数φ(C)越小,可知正反应为气体物质的量增大的反应,即n<p+q。
A. 催化剂只改变化学反应速率,对平衡移动没有影响,C的质量分数不变,故A错误;
B. 由上述分析可知,可逆反应mA(固)+nB(气)Pc(气)+qD(气)正反应为放热反应,升高温度平衡向吸热方向移动,即向逆反应移动,故B正确;
C. 由上述分析可知,可逆反应mA(固)+nB(气)Pc(气)+qD(气)正反应为气体物质的量增大的反应,即n<p+q,故C错误;
D.A为固体,浓度为定值,达平衡后,增加A的量,平衡不移动,故D错误。
答案选B。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某同学为探究苯和液溴的反应,设计了如下图所示实验装置进行。
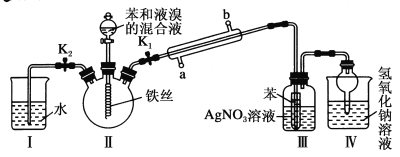
回答下列问题:
(1)冷凝管的进水口是________(填“a”或“b”)。
(2)关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。装置Ⅲ中小试管内苯的作用是______________。
(3)该实验能否证明苯和液溴发生了取代反应?_____(填“能”或“不能”),理由是______。
(4)反应结束后,关闭K1和分液漏斗活塞,打开K2,此时装置Ⅰ中的水倒吸入装置Ⅱ中,这样操作的目的是_____________。
(5)最后将三颈烧瓶内的液体依次进行下列实验操作就可得到较纯净的溴苯。
a.用蒸馏水洗涤,振荡,分液;
b.用5%的NaOH溶液洗涤,振荡,分液;
c.用蒸馏水洗涤,振荡,分液;
d.加入无水CaCl2粉末干燥;
e.________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“花卉保鲜剂”是一种可以延长花期的试剂。如表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(gmol1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.0075 | 170 |
(1)下列“花卉保鲜剂”的成分中,属于非电解质的是______,可做杀菌剂的是____
A. 高锰酸钾B. 硫酸钾C. 蔗糖D. 硝酸银E. 水
(2) 配制1L上述“鲜花保鲜剂”需要高锰酸钾______mol。
(3)在溶液配制过程中,下列操作会使配制结果无影响的是______。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚配制完一定物质的量浓度的氯化钠溶液未洗涤
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为______mol/L。
(5)如果用高铁酸钾(K2FeO4)代替高锰酸钾效果会更好,湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O.碱性条件下,氧化剂与还原剂的物质的量的比为3:2发生反应,写出并配平湿法制备高铁酸钾的离子反应方程式___________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
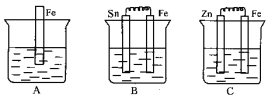
(1)A中反应的离子方程式为_________________________________。
(2)B中Fe极为_______极,电极反应式为_______________________。C中Fe极为_______极,电极反应式为__________________________,电子从_______极流出(填“Zn”或“Fe”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是一种重要的医药活性中间体,其合成路线如图:
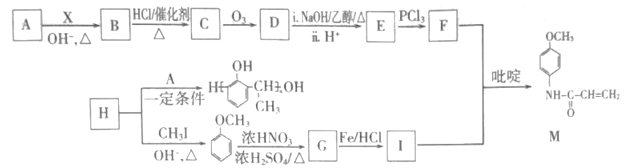
已知:ⅰ.2CH3CHO![]() CH3CH=CHCHO
CH3CH=CHCHO
ⅱ.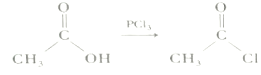
ⅲ.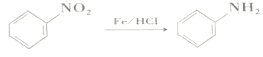 (在空气中极易被氧气氧化)
(在空气中极易被氧气氧化)
请回答以下问题:
(1)B中官能团名称为___,检验其官能团所需试剂先后顺序为___(填字母)。
a.银氨溶液 b.NaOH溶液 c.稀硫酸 d.稀盐酸 e.酸性高锰酸钾溶液
(2)F与I的反应类型是___,吡啶是一种有机碱,其作用为___。
(3)写出![]() 与A反应的化学方程式___。
与A反应的化学方程式___。
(4)N是G的同分异构体,写出满足下列条件N的两种结构简式___。
①苯环上的一氯代物有两种②含有两种官能团③能发生银镜反应
(5)写出以![]() 为原料制备
为原料制备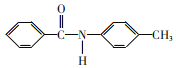 的合成路线(其它无机试剂任选)___。
的合成路线(其它无机试剂任选)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包白色粉末,由BaCl2、K2SO4、CaCO3、NaOH、CuSO4中的一种或几种组成,为了探究它的成份,进行了如下实验:下列判断正确的是( )

A. BaCl2,CaCO3一定存在,NaOH可能存在
B. K2SO4、CuSO4一定不存在
C. K2SO4、NaOH、CaCO3、BaCl2一定存在,CuSO4可能存在
D. C为单一溶质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.Zn+CuSO4=ZnSO4+CuB.3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
C.AgNO3+KCl=AgCl↓+KNO3D.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体并使其发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
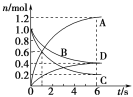
A. 该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B. 0~1 s内,v(A)=v(C)
C. 0~6 s内,B的平均反应速率为0.05 mol·L-1·s-1
D. 0~6 s内,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是常用的食品调味剂。
回答下列问题:
(1)写出元素D在周期表中的位置____________________________________________。
(2)五种元素中,原子半径最大的是________(填元素符号),非金属最强的是________(填元素符号)。
(3)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是________(用化学式表示)。
(4)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为________,其中存在的化学键类型为_______________和________________。
(5)单质E与水反应的离子方程式为____________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com