
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是常用的食品调味剂。
回答下列问题:
(1)写出元素D在周期表中的位置____________________________________________。
(2)五种元素中,原子半径最大的是________(填元素符号),非金属最强的是________(填元素符号)。
(3)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是________(用化学式表示)。
(4)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为________,其中存在的化学键类型为_______________和________________。
(5)单质E与水反应的离子方程式为____________________________________________
【答案】第三周期 第ⅤA族 Na Cl PH3 NH4Cl 离子键 共价键 Cl2+H2OH++Cl-+HClO
【解析】
五种短周期元素A、B、C、D、E的原子序数依次增大.A和B形成的共价化合物在水中呈碱性,该化合物为NH3,则A为氢元素、B为氮元素;A和C同族,C的原子序数大于氮元素,故C为Na元素;B和D同族,则D为磷元素;C和E形成的化合物是厨房中常见的物质,该物质为NaCl,则E为Cl元素,据此进行解答。
由分析知:A为氢元素、B为氮元素、C为Na元素、D为磷元素、E为Cl元素;
(1)元素D为磷元素,原子结构示意图为![]() ,则磷元素在周期表中的位置是第三周期第ⅤA族;
,则磷元素在周期表中的位置是第三周期第ⅤA族;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故Na元素的原子半径最大;最高价含氧酸的酸性越强,中心元素的非金属性越强,高氯酸是最强的含氧酸,故Cl非金属性最强;
(3)由A和B、D、E所形成的共价型化合物分别为NH3、PH3、HCl,非金属性越强氢化物越稳定,故热稳定性最差的是 PH3;
(4)A和E形成的化合物HCl,A和B形成的化合物NH3,二者反应生成NH4Cl,NH4Cl为离子化合物,存在的化学键类型为离子键和共价键;
(5)单质E为氯气,氯气与水反应生成盐酸与次氯酸,反应离子方程式为:Cl2+H2O![]() H++Cl-+HClO。
H++Cl-+HClO。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】可逆反应mA(固)+nB(气)![]() pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
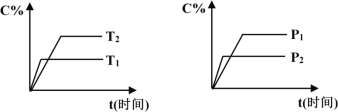
A. 达到平衡后,使用催化剂,C%将增大
B. 达到平衡后,若升高温度、化学平衡向逆反应方向移动
C. 方程式中n>p+q
D. 达到平衡后,增加A的量有利于化学平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH= +49.0kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
由上述方程式可知:CH3OH的燃烧热____(填“大于”“等于”或“小于”)192.9kJ/mol。已知水的气化热为44kJ/mol。则表示氢气燃烧热的热化学方程式为___。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH= +44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式___。
(3)已知:①Fe(s)+![]() O2(g)=FeO(s) ΔH1= -272.0kJ/mol
O2(g)=FeO(s) ΔH1= -272.0kJ/mol
②2Al(s)+![]() O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
Al和FeO发生铝热反应的热化学方程式是___。铝热反应的反应类型___,某同学认为,铝热反应可用于工业炼铁,你的判断是____(填“能”或“不能”),你的理由____。
(4)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃、101KPa下:
①H2(g)+![]() O2(g)=H2O(g) ΔH1= -242kJ/mol
O2(g)=H2O(g) ΔH1= -242kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是 ( )
A. 2H+(aq) +![]() (aq)+
(aq)+![]() (aq)+2
(aq)+2![]() (aq)=BaSO4(s)+2H
(aq)=BaSO4(s)+2H![]() O(1)
O(1) ![]() H=
H=![]() 114.6 kJ/mol
114.6 kJ/mol
B. 2KOH(aq)+ H![]() SO4(aq)= K
SO4(aq)= K![]() SO4(aq)+2H
SO4(aq)+2H![]() O(l)
O(l) ![]() H=
H=![]() 114.6kJ/mol
114.6kJ/mol
C. C8H18(l)+ ![]() O
O![]() (g)=8CO
(g)=8CO![]() (g)+ 9H
(g)+ 9H![]() O
O ![]() H=
H=![]() 5518 kJ/mol
5518 kJ/mol
D. 2C8H18(g)+25O![]() (g)=16CO
(g)=16CO![]() (g)+18H
(g)+18H![]() O(1)
O(1) ![]() H=
H=![]() 5518 kJ/mol
5518 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 向蛋白质溶液中加入醋酸铅溶液,产生白色沉淀 | 蛋白质发生了盐析 |
B | SO2通入Ba(NO3)2溶液中,产生白色沉淀 | 沉淀为BaSO3 |
C | 向蔗糖中加入适量浓硫酸并搅拌,蔗糖变黑,体积膨胀,并放出刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
D | 分别向等物质的量浓度的苯酚钠溶液和碳酸钠溶液中滴加酚酞,后者红色更深 | 碳酸酸性强于苯酚 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,3.36L氧气与3.2g硫反应,生成SO2分子数为0.1NA
B.1L0.1mol·L-1氨水中NH3·H2O分子数为0.1NA
C.标准状况下,1.12L氯气发生反应转移的电子数一定为0.1NA
D.46gNO2和N2O4混合气体中氧原子总数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一个五圆环,每个环中的物质依次为FeCl3、NaCl、Na2O2、CO2、I2,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
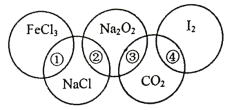
(1)关于上述相交部分的说法不正确的是___(填序号)。
A.①表示盐类 B.②表示钠的化合物
C.③表示氧化物 D.④表示非电解质
(2)关于上述相交部分的说法正确的是___(填序号)。
A.海水晒盐属于物理变化 B.Na2O2属于碱性氧化物
C.I2易溶于CCl4 D.钠着火可用CO2灭火
(3)若NaCl固体中含有少量I2杂质,可采用的除杂方法是___(填序号)
A.过滤 B.加热 C.渗析
(4)上述五种物质中,有两种物质可以发生氧化还原反应,其化学方程式为___;
(5)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1mol·L-1图中某物质M的溶液,继续煮沸得到红褐色透明液体。
①物质M的化学式为____。
②检验该红褐色透明液体是胶体的方法为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当密闭容器中合成氨反应N2+3H2![]() 2NH3达到平衡后,保持温度不变,将容器的容积压缩为原来的1/2。达到新平衡后,与原平衡相比较,下列说法中正确的是
2NH3达到平衡后,保持温度不变,将容器的容积压缩为原来的1/2。达到新平衡后,与原平衡相比较,下列说法中正确的是
A. 容器内的总压强为原来的2倍 B. N2的浓度比原来平衡浓度小
C. H2的转化率为原来的2倍 D. 气体的密度为原来的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的铁、镁和铜的混合物与一定量的浓HNO3恰好反应,得到硝酸盐溶液和NO2、N2O4、NO的混合气体,这些气体与2.24L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸.若向所得硝酸盐溶液中加入2mol/L的NaOH溶液至Fe3+、Mg2+、Cu2+恰好沉淀,则消耗NaOH 溶液的体积是( )
A.400 mL B.200 mL C.150 mL D.80 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com