
【题目】某课题组设计如图所示实验装置探究H2S的制法和性质。若装置A产生的是有臭鸡蛋气味的硫化氢气体,则下列说法错误的是( )

A.装置B中的现象可证明溴的非金属性比硫强
B.酸X可以是稀硝酸
C.装置C中的现象可证明CuS难溶于稀硫酸
D.能观察到装置D中溶液的红色变浅
科目:高中化学 来源: 题型:
【题目】在一定温度下,在1L密闭容器中加amolSO2和bmolO2发生反应2SO2+O2![]() 2SO3,反应达到平衡时有cmolSO2发生了反应,试填下列空白:
2SO3,反应达到平衡时有cmolSO2发生了反应,试填下列空白:
(1)生成___molSO3;
(2)O2的转化率为___;
(3)平衡时容器内气体的总物质的量为___mol;
(4)达到平衡时,c(SO2)=___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.氯气有氧化性,可使干燥布条漂白褪色
B.常温下,铁、铝不与浓硫酸反应,因此可用铁、铝容器贮存运输浓硫酸
C.已知电离能力H2CO3>HClO>![]() ,则向氯水中加入碳酸氢钠晶体,能提高溶液中HClO的浓度
,则向氯水中加入碳酸氢钠晶体,能提高溶液中HClO的浓度
D.向BaCl2溶液中通入SO2可产生白色浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丹参醇是存在于中药丹参中的一种天然产物。合成丹参醇的部分路线如下:
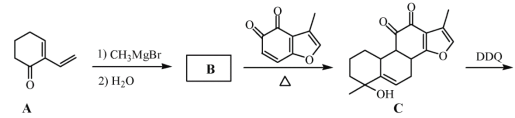
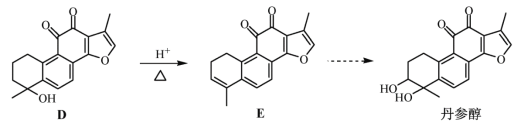
已知:![]() 。
。
(1)A中的官能团名称为_________、_________(写两种)。
(2)D![]() E的反应类型为__________________。
E的反应类型为__________________。
(3)B的分子式为C9H14O,写出B的结构简式:__________________。
(4)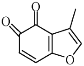 的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_________。
的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_________。
①分子中含有苯环,能与FeCl3溶液发生显色反应,不能发生银镜反应;
②碱性条件水解生成两种产物,酸化后分子中均只有2种不同化学环境的氢。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为装有活塞的密闭容器,内盛22.4 mL一氧化氮。若通入11.2 mL氧气(气体体积均在标准状况下测定)保持温度、压强不变,则容器内气体的密度( )
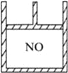
A. 等于1.369 g/LB. 等于2.054 g/L
C. 在1.369 g/L和2.054 g/L之间D. 大于2.054 g/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某甲烷燃料电池构造示意图如图所示,关于该电池的说法不正确的是
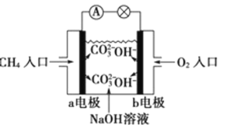
A.应该甲烷燃料电池的总反应:CH4+2O2=CO2+2H2O
B.正极的电极反应是:O2+2H2O+4e-=4OH-
C.a极是负极,发生氧化反应
D.甲烷燃料电池是环保电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:
①N2O5(g) ![]() N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g) ![]() N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2 L的密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol。则平衡体系中N2O5的物质的量浓度为
A. 1.8mol/L B. 0.9 mol/L C. 2.3 mol/L D. 4.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种常见的化工原料。查阅资料知:苯和液溴在溴化铁(FeBr3)存在的条件下可发生反应生成溴苯,此反应为放热反应。实验室合成溴苯的装置示意图及有关数据如下。先向A中加入16.0mL的无水苯和5.0mL液溴,再将混合液慢慢滴入反应器B中。请回答下列问题:
苯 | 溴 | 溴苯 | |
相对分子质量 | 78 | 160 | 157 |
颜色状态 | 无色液体 | 深红棕色液体 | 无色液体 |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中的溶解性 | 难溶 | 微溶 | 难溶 |

(1)仪器A的名称为____。
(2)反应器B中发生的主要有机反应的化学方程式是___。
(3)下列关于该实验操作或叙述错误的是___(填字母序号)。
a.向反应器B中滴加苯和溴的混合液前需先关闭K
b.实验中装置C中的液体逐渐变为浅红色
c.实验中装置D中的导管口附近有白雾产生,溶液中产生淡黄色的沉淀,根据该现象说明苯和液溴发生的反应为加成反应
d.装置D中的导管不能插入液面以下和装置E中导管末端连接倒扣着的漏斗都是为了防倒吸
e.溴苯不能与AgNO3溶液反应产生淡黄色沉淀
(4)实验完毕待冷却后,经过下列步骤对溴苯进行分离提纯:
①向B中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。用NaOH溶液洗涤的作用是___;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
(5)经过上述分离操作后,粗溴苯中还含有的主要杂质为__,要进一步提纯,下列操作中必须的是___。
a.萃取 b.蒸馏 c.重结晶 d.过滤 e.分液
(6)若经过上述分离提纯的操作,经进一步精制得到6.2mL的溴苯,则该实验中溴苯的产率是___(计算结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关①100mL 0.1 mol/L![]() 、②100mL 0.1 mol/L
、②100mL 0.1 mol/L![]() 两种溶液的叙述不正确的是
两种溶液的叙述不正确的是
A.溶液中水电离出的![]() 个数:②>①B.溶液中阴离子的物质的量浓度之和:②>①
个数:②>①B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:![]() D.②溶液中:
D.②溶液中:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com