
����Ŀ��ʵ�����ò�����Ũ���ᷴӦ�Ʊ�CO,��ԭ�����£�H2C2O4![]() CO��+CO2��+H2O��ij������ͬѧ���ʵ��̽��CO��ԭ����Ǧ(��ɫ��ĩ)��������������(��֪CO��ʹ������Һ������ɫ����),װ����ͼ��ʾ��
CO��+CO2��+H2O��ij������ͬѧ���ʵ��̽��CO��ԭ����Ǧ(��ɫ��ĩ)��������������(��֪CO��ʹ������Һ������ɫ����),װ����ͼ��ʾ��
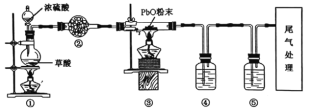
����˵����ȷ���ǣ� ��
A. �ڡ��ܡ������Լ�����Ϊ��ʯ�ҡ�������Һ������ʯ��ˮ
B. ����������������������������ʱ˵�����п������ž�
C. ʵ�����ʱ,��Ϩ��ٴ��ƾ���,��Ϩ��۴��ƾ���
D. ʵ������й۲쵽�۲������л�ɫ��ĩ��ɰ�ɫ��ĩ
���𰸡�B
��������
A.װ���Т���Ҫ����CO��CO2��H2O������Ϊ��ʯ�����ڳ�ȥCO2��H2O �����з�����Ӧ��PbO+CO![]() CO2+Pb�������ó���ʯ��ˮ���鲢��ȥ��Ӧ�����ɵ�CO2��������������Һ����װ�����Ƿ������CO�����Т������������Լ�����Ϊ��ʯ�ҡ�����ʯ�ҡ�ˮ������Һ����A����B.������������������������������ʱ˵�����п������ž�����B��ȷ��C.ʵ�����ʱ,��Ϩ��۴��ƾ���,��Ϩ��ٴ��ƾ��ƣ��Է�������������C����D.һ��������ֳ�����ɫ���������ڷ�ĩ״Ϊ�Һ�ɫ����D����ѡB��
CO2+Pb�������ó���ʯ��ˮ���鲢��ȥ��Ӧ�����ɵ�CO2��������������Һ����װ�����Ƿ������CO�����Т������������Լ�����Ϊ��ʯ�ҡ�����ʯ�ҡ�ˮ������Һ����A����B.������������������������������ʱ˵�����п������ž�����B��ȷ��C.ʵ�����ʱ,��Ϩ��۴��ƾ���,��Ϩ��ٴ��ƾ��ƣ��Է�������������C����D.һ��������ֳ�����ɫ���������ڷ�ĩ״Ϊ�Һ�ɫ����D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̽��������ˮ�ɷּ����ʵ�ʵ���У��������з������������ܵó���Ӧ���۵���
���� | ���� | ���� | |
A | �۲���ˮ��ɫ | ��ˮ�ʻ���ɫ | ��ˮ�к�Cl2 |
B | ��NaHCO3��Һ�м���������ˮ | ����ɫ������� | ��ˮ�к�HClO |
C | ���ɫֽ���ϵμ���ˮ | ��ɫֽ����ɫ | ��ˮ����Ư���� |
D | ��FeCl2��Һ�еμ���ˮ | ��Һ����ػ�ɫ | ��ˮ���������� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϵ�е�һ��Ԫ�أ�1 mg�(![]() )ÿ����Լ���ͷų�2.34��109�����ӣ���ҽѧ�ϳ��������ƶ�������������Դ�������й�˵��������� �� ��
)ÿ����Լ���ͷų�2.34��109�����ӣ���ҽѧ�ϳ��������ƶ�������������Դ�������й�˵��������� �� ��
A. ![]() �У��������͵�������Ϊ98 B.
�У��������͵�������Ϊ98 B. ![]() ��
��![]() ��Ϊͬλ��
��Ϊͬλ��
C. �λ��Ԫ�����ڱ��������� D. ![]() ����������������֮��Ϊ56
����������������֮��Ϊ56
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4���ƵĻ�����W��X��Y��Z������֮��������¹�ϵ��
��W![]() X��H2O��CO2������Z��CO2�D��X��O2
X��H2O��CO2������Z��CO2�D��X��O2
��Z��H2O�D��Y��O2������X��Ca(OH)2�D��Y��CaCO3��
�Իش��������⣺
��1��W��X��Y��Z�Ļ�ѧʽ�ֱ���W__________��X__________��Y__________��Z__________��
��2������4����ѧ��Ӧ������������ԭ��Ӧ����________(�Ӧ���)����Ӧ�е���������____________(д��ѧʽ)����ԭ����____________(д��ѧʽ)��
��3������Ӧ������Һ�н��У�д�������ӷ���ʽ�Լ����ø����ӷ���ʽ��ʾ����һ����ѧ��Ӧ�Ļ�ѧ����ʽ��
�����ӷ���ʽ��________________��
�ڻ�ѧ����ʽ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л����˵����ȷ���ǣ� ��
A. ��ά�ء�����ˮ������ղ�����ͬ
B. ��ϩ��������Ȼ�̼��Һ��Ӧ����1,3-�������
C. ![]() ��������16��ԭ�ӹ�ƽ��
��������16��ԭ�ӹ�ƽ��
D. ![]() �ı�����һ�ȴ�����3��
�ı�����һ�ȴ�����3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijЩ����ũҩ�����õ��ԭ�������й�Ʒ�İ�ȫ����,�����ũҩ��������ɵ���̬������Σ����������ȷ���ǣ� ��
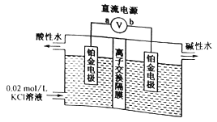
A. aΪֱ����Դ�ĸ�������֮�����ĵ缫������ B. ���ӽ���ĤΪ�����ӽ���Ĥ
C. ������ˮ������ǿ������,����ɱ��Ч�� D. ������ӦʽΪ��H2O--2e-=H2��+O2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ֲ���纣���������к��зḻ�ĵ�Ԫ�ء��Ӻ�������ȡ��Ĺ�ҵ������������,����˵����������

A. ���̢ٵķ��뷽���ǹ��ˣ���Ҫ�õ��IJ���������©�������������ձ�
B. ����NaOH��Һ��Ŀ����ʹ�������л����γɳ���
C. �����������п���ѡ����ˮ��Ϊ������
D. ���̢��ڹ�ҵ�ϳ�������ȡ��Һ�ķ����õ��ⵥ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ͭ��Ũ��������ڼ��������·������·�Ӧ(��Ӧ����ʽ����ƽ)��Cu+2H2SO4(Ũ)![]() CuSO4+A��+2H2O���������������⣺
CuSO4+A��+2H2O���������������⣺
(1)A���ʿ��Ե���������γɡ���AӦ������______(����ĸ������д)
a���� b�� �� c���� d������������ e������������
(2)�÷�Ӧ�б�������Ԫ����_________________���μӷ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ______��
(3)д���÷�Ӧ�Ļ�ѧ����ʽ����˫���ű������ת�Ƶķ������Ŀ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ǧ���ص��ܷ�ӦʽΪ��PbO2+Pb+2H2SO4![]() 2PbSO4+2H2O�ݴ��ж�����������ȷ���ǣ� ��
2PbSO4+2H2O�ݴ��ж�����������ȷ���ǣ� ��
A. �ŵ�ʱ��H2SO4Ũ������
B. �ŵ�ʱ�������ĵ缫��ӦʽΪ��Pb+SO42����2e���TPbSO4
C. �ڳ��ʱ�������ÿת��1 mol���ӣ�����������2 mol����
D. �ڳ��ʱ�����������ķ�Ӧ��PbSO4��2e��+2H2O�TPbO2+SO42��+4H+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com