
| 滴定 次数 | 待测溶液的体积 /mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.实验室加热高锰酸钾制氧气时,用排水法收集氧气出现倒吸现象,立即松开试管上的橡皮塞 |
| B.在气体发生装置上直接点燃氢气时,必须先检验氢气的纯度 |
| C.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 |
| D.给试管中的液体加热时不停移动试管或加入碎瓷片,以免暴沸伤人 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
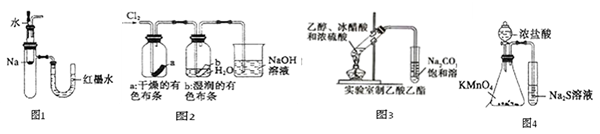
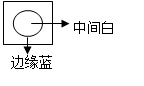
| A.图1中:将胶头滴管中的水滴入到金属钠中,能看到U型管右侧红墨水上升 |
| B.图2中:观察到湿润的有色布条能退色,待尾气全部被碱吸收后,将稀硫酸滴入烧杯中,至溶液显酸性,可能看到有黄绿色气体生成。 |
| C.图3可用于制备乙酸乙酯 |
D.图4可以比较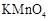 、 、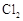 和S氧化性的相对强弱 和S氧化性的相对强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
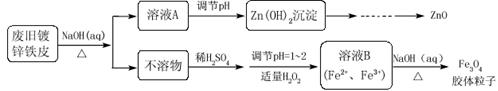
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分液操作时分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B.容量瓶使用前需要检查是否漏水 |
| C.配置0.1000 mol·L—1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流 |
| D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②⑤ | B.③⑤⑥ | C.①②④ | D.③④⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
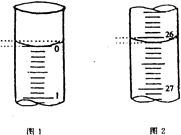
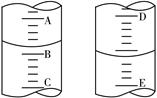
| A.用25mL碱式滴定管量取20.00mLNaHCO3 |
| B.用托盘天平准确称量10.20克碳酸钠固体 |
| C.用100mL量筒量取3.2mL浓硫酸 |
| D.配制1 mol·L–1的氢氧化钠溶液475mL选用500mL容量瓶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
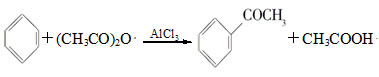
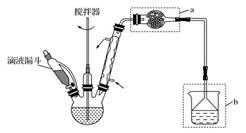
| A.反应太剧烈 | B.液体太多搅不动 | C.反应变缓慢 | D.副产物增多 |
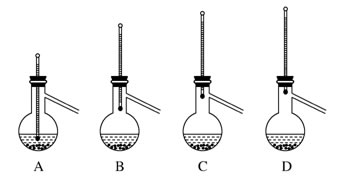
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com