
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为 。
(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
(1)、第三周期第ⅢA族(2分)
(2)、①4Al+3O2+6H2O=4Al(OH)3 (2分)
②增强溶液的导电能力(2分)
③I-+3H2O-6e-=IO3-+6H+ (2分) ④2.7g (2分)
【解析】
试题分析::(1)、铝元素核电荷数为13,在第三周期第IIIA族;(2)、①空气中氧气及水和铝反应生成氢氧化铝,反应方程式为:4Al+3O2+6H2O=4Al(OH)3,②溶液中离子浓度越大,离子所带电荷越多,溶液的导电性越强。加入氯化钠,增大了自由移动离子的浓度,水的导电性增强;
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极I—放电,其电极反应式为I-+3H2O-6e-=IO3-+6H+ ④由关系式:
2Al ---- 6OH-
2×27g 6mol
m/50% 0.5L×0.3 mol·L-1解得m=2.7g
(3)、①氯化铝在加热条件下易升华,因此判断氯化铝为共价化合物且各原子核外为8电子稳定结构所以其结构式为:
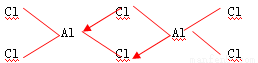
②加热条件下,氯气、氧化铝和碳反应生成氯化铝和一氧化碳,反应方程式为:
Al2O3+3C+3Cl2 =2AlCl3+3CO.
考点:了解原电池的工作原理,能写出电极反应和电池反应方程式。了解金属、非金属在元素周期表中的位置及其单质、化合物的性质和应用。


科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末教学质量检测化学试卷(解析版) 题型:选择题
与100 mL 0.1mol/L (NH4)2SO4溶液中c(NH4+)基本相同的是
A.200 mL 0.1 mol/L NH4Cl 溶液 B.50 mL 0.2 mol/L NH4NO3溶液
C.100 mL 0.2 mol/L NH4HSO4 D.50 mL 0.2 mol/L氨水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三12月月考化学试卷(解析版) 题型:选择题
关于Li、Na、K、Rb、Cs的叙述均正确的一组是
①金属性最强的是铯 ②它们的氧化物都只有M20和M202两种形式
③在自然界中均以化合态形式存在 ④密度按Li—Cs顺序依次递增
⑤离子半径:Rb+>K+>Na+
A.①②③ B.①③④⑤ C.②④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三1月练习理综化学试卷(解析版) 题型:实验题
(14分)常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料。某探究小组利用下列反应和装置制备一硝基甲苯。

实验中可能用到的数据:

实验步骤:①按体积比1:3配制浓硫酸与浓硝酸混合物40 mL;
②在三颈瓶中加入15 mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60 g。
请回答下列问题:
配制混酸的方法是_____ ___。
反应中需不断搅拌,目的是_________________________________________________。
(2)仪器A的名称是________,使用该仪器前必须进行的操作是_________。
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是_________。
(4)分离反应后产物的方案如下:

其中,操作1的名称为________,操作2中需要使用下列仪器中的________(填序号)。
a.冷凝管
b.酒精灯
c.温度计
d.分液漏斗
e.蒸发皿
(5)该实验中一硝基甲苯的产率为________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三1月练习理综化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关。对下列现象或事实解释错误的是
选项 | 现象或事实 | 解释 |
A | 明矾用于净水 | 铝离子水解产生的胶体具有很强吸附杂质的作用 |
B | SO2能使品红溶液褪色 | SO2具有漂白性 |
C | “地沟油”禁止食用,但可以用来制肥皂 | “地沟油”主要成分为油脂属于酯类可以发生皂化反应 |
D | 用氯水和淀粉溶液鉴别食盐是否加碘 | 目前加碘食盐中含碘元素物质为KI |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省等五校高三上学期第二次联考理综化学试卷(解析版) 题型:选择题
X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20,下列判断正确的是
W | X | Y |
Z |
A. 四种元素的原子半径:rZ>rX>rY>rW
B. 四种元素形成的单质最多有6种
C. 四种元素均可与氢元素形成电子总数为18的分子
D. 四种元素中,Z的最高价氧化物对应的水化物酸性最强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三第五次调研考试化学试卷(解析版) 题型:填空题
(14分)某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO4。已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。

部分阳离子以氢氧化物形式沉淀时的pH如下:

(1)“碱浸”过程中发生反应的离子方程式是
(2)“酸浸”时所加入的酸是 (填化学式)。
(3)加入H2O2时发生反应的离子方程式为
(4)操作b为调节溶液的pH,你认为pH的调控范围是
(5)产品晶体中有时会混有少量绿矾(FeS04·7H20),其原因可能是 (写出一点即可)。
(6)NiS04·7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三第三次调研考试化学试卷(解析版) 题型:选择题
下列有关原电池和电解池的叙述中,正确的是
A.纯锌与稀硫酸的反应比Zn-Cu合金与稀硫酸的反应更快
B.钢铁发生吸氧腐蚀时,负极的反应式为:Fe-3e-=Fe3+
C.在铁制容器上镀铜时,铁制容器连接外接电源的正极
D.电解精炼铜时,阴极的电极反应为:Cu2+ + 2e-=Cu
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省濉溪县高三第二次月考化学试卷(解析版) 题型:选择题
下列有关离子方程式书写正确的是
A.Fe(NO3)3溶液中加入少量的HI溶液:2Fe3++2I-=2Fe2++I2
B.向Mg(HCO3)2溶液中加入过量NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O
C.用惰性电极电解饱和食盐水:2Cl-+2H+ H2↑+Cl2↑
H2↑+Cl2↑
D.向苯酚钠溶液中通入少量的CO2:2C6H5O--+CO2 +H2O=2C6H5OH+CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com