
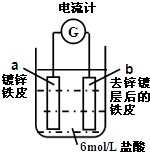
| A、a为阴极,铁皮受到保护 |
| B、盐酸中的Cl-向b定向移动 |
| C、在两个电极反应中,锌元素分别被氧化或被还原 |
| D、锌镀层完全溶解之时,电流计指针几乎没有偏转 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| a | |||||||||||||||||
| f | h | m | |||||||||||||||
| b | d | g | l | ||||||||||||||
| c | e | ||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3- |
| B、CO32- |
| C、H+ |
| D、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L的H2O所含的分子数为NA |
| B、1mol T2O分子所含的中子数为10NA |
| C、常温常压下,20g D2O分子中所含的质子数为10NA |
| D、1mol H3O+所含的电子数为11NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、还原剂 |
| B、氧化剂 |
| C、既是氧化剂又是还原剂 |
| D、既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 按某一分类标准分类的一组 | 归类 |
| A | FeSO4 、NO2 、MnO2、NaClO | H2SO3 |
| B | CH3COOH、HClO、H2S、HOOC-COOH | HF |
| C | 加聚反应、离子反应、放热反应、氧化还原反应 | 焰色反应 |
| D | (NH4)2SO4、NH4Cl、NH4NO3、NH3?H2O | NH4HCO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、2s的电子云模型是: |
B、肽键的结构式为: |
C、H2S分子的球棍模型为: |
D、最外层电子排布式为ns2np3对应的轨道表示式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯和环丙烷(C3H6)组成的28g混合气体中含有3NA个氢原子 |
| B、1mol碳酸钾晶体中含阴离子数为NA 个 |
| C、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
| D、将0.1mol氯化铁溶于1L水中,所得溶液中含有0.1NA Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com