
(物质结构与性质)化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层中P轨道上的电子数等于前一电子层电子总数,X原子最外层的P轨道中有一个轨道填充了2个电子。则
(1)X原子的电子排布式是 ,Y原子的价层电子轨道表示式是
(2)YX2的分子构型是 ,YX2的熔沸点比ZX2 ,(选填“高”或“低”),理由是
(3)YX2分子中,Y原子的杂化类型是 ,一个YX2分子中含 个![]() 键。
键。
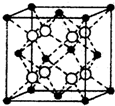
(4)下图表示一些晶体的结构(晶胞),其中代表YX2的是

(1) ![]() ,
,![]() (2) 直线型,低⑶SP杂化,2个∏键⑷B
(2) 直线型,低⑶SP杂化,2个∏键⑷B
根据题意:Y元素的最外层中P轨道上的电子数是前一电子层电子总数,因为P轨道最多能排6个电子﹤8,则Y元素只有两个电子层,且最外层P轨道上只有2个电子,其最外层共有4个电子,Y元素为碳元素,Z与Y同主族,Z为硅元素,X与Y同周期,则X有2个电子层,X原子最外层P轨道上有一个轨道填充了2个电子,依据电子排布规律可知P轨道共有4个电子。则X为氧元素。问题⑴:根据核外电子排布规律可以写出X原子的核外电子排布式为![]() ,Y原子的价层电子轨道表示式为:
,Y原子的价层电子轨道表示式为:![]()
问题⑵:YX2分子是CO2 ,分子构型是直线型分子,ZX2是SiO2,因为CO2 是分子晶体,SiO2是原子晶体,所以CO2 的熔点比SiO2的熔点低。
问题⑶YX2是CO2 ,由CO2分子是直线型分子可以推断出CO2 分子中C原子的杂化类型是SP杂化。CO2 分子内的共价键是碳氧双键(C=O),每一个双键中有1个∏键,共有2个∏键。
问题⑷CO2 属于分子晶体,结合选项可以选出其晶体结构是B。


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2013?烟台一模)【化学--物质结构与性质】
(2013?烟台一模)【化学--物质结构与性质】查看答案和解析>>
科目:高中化学 来源: 题型:
[化学——选修3:物质结构与性质](15分)
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
请回答下列问题:

(1)由B2O3制备BF3、BN的化学方程式依次是 、 ;
(2)基态B原子的电子排布式为 ;B和N相比,电负性较大的是 ,BN中B元素的化合价为 ;
(3)在BF3分子中,F—B—F的键角是 ,B原子的杂化轨道类型为 ,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为 ;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为 ,层间作用力为 ;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm。立方氮化硼晶胞中含有______个氮原子、______个硼原子,立方氮化硼的密度是______ g·cm-3(只要求列算式,不必计算出数值。阿伏伽德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学——选修3:物质结构与性质]
拟化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BP3和BN,如下图所示:

请回答下列问题:
(1) 由B2O3制备BF3、BN的化学方程式依次是_________、__________;
(2) 基态B原子的电子排布式为_________;B和N相比,电负性较大的是_________,BN中B元素的化合价为_________;
(3) 在BF3分子中,F-B-F的建角是_______,B原子的杂化轨道类型为_______,BF3和过量NaF作用可生成NaBF,BF的立体结构为_______;
(4) 在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________,层间作用力为________;
(5)六方氢化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶苞边长为361.5pm,立方氮化硼晶苞中含有______各氮原子、________各硼原子,立方氮化硼的密度是_______g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com