
| A、制半导体材料的元素 |
| B、制农药的元素 |
| C、制催化剂的元素 |
| D、制耐高温合金的元素 |
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:

| 离子 | Fe3+ | Cu2+ | Zn2+ |
| 完全沉淀时的pH | 3.2 | 6.7 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过滤时,用玻璃棒搅动漏斗内液体,使之过滤完全 |
| B、燃着的酒精灯打翻失火,应立即用水浇灭 |
| C、配制一定浓度的NaCl溶液时,定容振荡摇匀后,发现液面低于刻度线,再加水到刻度线 |
| D、浓硫酸不慎溅到皮肤上,应立即用大量水冲洗,最后再涂上3%~5%的小苏打溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①④ | C、②③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
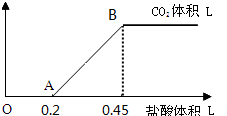
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.7g |
| B、23.4 g |
| C、35.1g |
| D、58.5g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com