
【题目】下列变化中,气体被还原的是 ( )
A.二氧化硫使酸性高锰酸钾溶液褪色B.氯气使KBr溶液变黄
C.二氧化碳使Na2O2固体变白D.氨气使MgCl2溶液产生白色沉淀
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】Na2S溶液中各种离子的物质的量浓度关系不正确的是( )
A. c(Na+)>c(S2-)>c(OH-)>c(HS-) B. c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-)
C. c(Na+)=2c(HS-)+2c(S2-)+2c(H2S) D. c(OH-)=c(H+) + c(HS-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国丝绸有五千年的历史和文化.古代染坊常用某种“碱剂”来精炼丝绸,该“碱剂”的主要成分是一种盐,能促进蚕丝表层的丝胶蛋白杂质水解而除去,使丝绸颜色洁白、质感柔软、色泽光亮.这种“碱剂”可能是( )
A.食盐
B.火碱
C.草木灰
D.胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中大量存在以下五种离子NO ![]() 、SO
、SO ![]() 、Al3+、H+、M.其物质的量浓度之比为c(NO
、Al3+、H+、M.其物质的量浓度之比为c(NO ![]() ):c(SO
):c(SO ![]() ):c(Al3+):c(H+):c(M)=4:3:1:3:2,则M可能是( )
):c(Al3+):c(H+):c(M)=4:3:1:3:2,则M可能是( )
A.Fe2+
B.Cl﹣
C.Mg2+
D.Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象描述正确的是

A. 逸出气体的体积,a电极的小于b电极的
B. 一电极逸出无味气体,另一电极逸出刺激性气体
C. a电极附近呈红色,b电极附近呈蓝色
D. a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,2gH2含有的氢原子数目为2NA
B.标准状况下,22.4LCCl4中含有的分子数为NA
C.标准状况下,20gD2O中含有的电子数为10NA
D.常温常压下,1molL﹣1K2CO3溶液中含有的钾离子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为molL﹣1 .
(2)现用该浓盐酸配制100mL 1molL﹣1的稀盐酸.可供选用的仪器有:
①胶头滴管 ②烧瓶 ③烧杯 ④药匙
⑤量筒 ⑥托盘天平
配制稀盐酸时,上述仪器中需要使用的有(选填序号),还缺少的仪器有(写仪器名称).
(3)配制100mL 1molL﹣1的稀盐酸需要用量筒量取上述浓盐酸的体积为mL(保留一位小数),量取浓盐酸时应选用(选填①10mL ②50mL ③100mL)规格的量筒.
(4)实验中造成所配溶液浓度偏高的原因可能是 .
A.未经冷却,立即转移至容量瓶并洗涤烧杯,定容
B.用量筒量取液体时仰视读数
C.烧杯没有洗涤
D.某同学在定容观察液面时俯视
E.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
F.容量瓶中原来含有少量蒸馏水.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡,根据要求回答下列问题:
(1)向 ZnSO4溶液中滴加饱和H2S溶液,没有沉淀生成,继续滴加一定量的氨水后,生成ZnS沉淀,用电离平衡原理解释上述现象 _______________________________________________ 。
(2)AlCl3溶液蒸干并灼烧得到的物质是__________ (填化学式)。
(3)0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为_____________。
(4)0.1mol·L-1的NaHA溶液中,粒子浓度由大到小的顺序为:c(Na+)>c(HA—)>c(H2A)>c(A2-)
①该溶液中显________(填“酸性”、“碱性”或“中性”);
②作出上述判断的依据是___________________________________________(用文字解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(I)甲烷在一定条件下可生成以下微粒:
A.碳正离子(CH3+ ) B.碳负离子(CH3﹣) C.甲基 (﹣CH3) D.碳烯(:CH2)
①四种微粒中,键角为120°的是(填序号).
②碳负离子(CH3﹣)的空间构型为 , 与CH3﹣互为等电子体的一种分子是(填化学式).
(II )在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒.除去CO的化学方程式为(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac.请回答下列问题:
①C、N、O的电负性由大到小的顺序为 .
②写出Cu的核外电子排布式 .
③化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为 .
④在一定条件下NH3和CO2能合成尿素CO(NH2)2 , 尿素中C原子轨道的杂化类型为;1mol尿素分子中,σ 键的数目为 .
⑤Cu2O晶体的晶胞结构如图所示,若阿伏伽德罗常数为NA , 晶胞的边长为apm,则晶体的密度为gcm﹣3 . 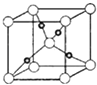
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com