
【题目】下列可以证明2HI(g)![]() H2(g)+I2(g)已达平衡状态的是( )
H2(g)+I2(g)已达平衡状态的是( )
①单位时间内生成nmolH2的同时生成nmolHI
②一个H—H键断裂的同时有两个H—I键断裂
③温度和体积一定时,混合气体密度不再变化
④v(H2)=v(I2)=0.5v(HI)
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧温度和压强一定时,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
A. ②③④⑤⑥B. ②⑥⑦⑧⑨
C. ①②⑥⑧D. ②⑥⑨
【答案】D
【解析】
①单位时间内生成nmolH2的同时生成nmolHI,说明正反应速率大于逆反应速率,反应未达到平衡;
②H—H键断表示逆反应反向,H—I键断裂表示正反应方向,一个H—H键断裂的同时有两个H—I键断裂,表示正逆反应速率相等,可以说明反应达到平衡;
③温度和体积一定时,反应前后的体积不变,所以混合气体密度始终不变,所以不能说明反应达到平衡;
④v(H2)=v(I2)=0.5v(HI),没有说明反应的方向,故不能说明反应达到平衡;
⑤c(HI):c(H2):c(I2)=2:1:1,不能说明反应物或生成物浓度不再变化,不能说明反应达到平衡;
⑥温度和体积一定时,某一生成物浓度不再变化,说明某物质的生成速率等于其消耗速率,也就是正反应速率等于逆反应速率,能说明反应达到平衡;
⑦温度和体积一定时,反应前后气体体积不变,所以压强始终不变,故压强不变时,不能说明反应达到平衡;
⑧温度和压强一定时,反应前后气体的总物质的量不变,根据质量守恒,混合气体的平均相对分子质量始终不变,故混合气体的平均相对分子质量不再变化不能说明反应达到平衡;
⑨温度和体积一定时,混合气体中只有I2有颜色,所以颜色不变说明物质浓度不变,能说明反应达到平衡,
故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】铵明矾NH4Al(SO4)2·12H2O是分析化学常用基准试剂,其制备过程如下。下列分析不正确的是

A. 过程Ⅰ反应:2NH4HCO3+Na2SO4===2NaHCO3↓+(NH4)2SO4
B. 检验溶液B中阴离子的试剂仅需BaCl2溶液
C. 若省略过程Ⅱ则铵明矾产率明显减小
D. 向铵明矾溶液中逐滴加入NaOH溶液先后观察到:刺激性气体逸出→白色沉淀生成→白色沉淀消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学称取9.00g淀粉溶于水,测定淀粉的水解百分率.其程序如下:
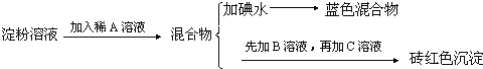
试回答下列问题:
(1)各步加入的试剂为:A_________,B_________,C_________;
(2)加入A溶液而不加入B溶液是否可以_________,其理由是_________;
(3)写出淀粉水解的方程式_________;
(4)当析出1.44g砖红色沉淀时,淀粉水解率是_________;[已知葡萄糖与Cu(OH)2反应的化学方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2![]() CH2OH(CHOH)4COOH+Cu2O↓+2H2O]。
CH2OH(CHOH)4COOH+Cu2O↓+2H2O]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取.收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中 A.B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位,请回答问题:
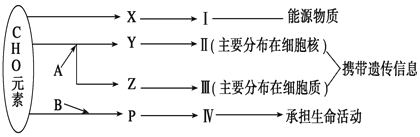
(1)图中X被形容为“生命的燃料”,它是____________,Ⅰ在小麦种子中主要是指____________。
(2)A和B各表示__________ 元素 和______________元素。
(3)Y完全水解的产物是__________、 _____________ 和 ________________。
(4)P的结构通式是____________________,P的种类有_____________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“![]() =
=![]() ”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。

下列叙述中正确的是( )
A. 甲组操作时,电流表(A)指针发生偏转
B. 甲组操作时,溶液颜色变浅
C. 乙组操作时,C2作正极
D. 乙组操作时,C1上发生的电极反应为I2+2e-===2I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学选3——物质结构与性质)利用 合成的新型三元催化剂[La0.8Cu0.2Ni1-xMxO3(M 分别为Mn、Fe和Co)]可以使汽车尾气中NO和CO发生反应而减少尾气污染,同时可大大降低重金属的用量。回答下列问题:
合成的新型三元催化剂[La0.8Cu0.2Ni1-xMxO3(M 分别为Mn、Fe和Co)]可以使汽车尾气中NO和CO发生反应而减少尾气污染,同时可大大降低重金属的用量。回答下列问题:
(1)Mn2+的核外电子排布式为:________________,其单电子数为_________________。
(2)C、N、O、Mn电负性由大到小的顺序是___________。
(3)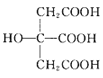 也是常见配体,其中采取sp2杂化的碳原子和sp3杂化的碳原子个数比为_____。
也是常见配体,其中采取sp2杂化的碳原子和sp3杂化的碳原子个数比为_____。
(4)蓝色物质KFe(Ⅲ)x[Fe(Ⅱ)(CN)6]可缓解重金属中毒,x=_______;该物质中不存在的作用力有_____。
A.范德华力 B.离子键 C.σ键 D.π键 E.氢键
(5)副族元素钴的氧化物可以在室温下完全氧化甲醛(HCHO)。甲醛分子的立体构型为_____;甲醛常温下为气体而甲醇(CH3OH)为液体的原因是________________________________ 。
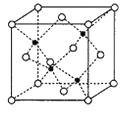
(6)副族元素Mn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中(○为Se,![]() 为Mn),该化合物的化学式为________,Se的配位数为______,Mn和Se的摩尔质量分别为M1g/mol、M2g/mol,该晶体的密度为ρg/cm3,则Mn—Se键的键长为_____________nm(计算表达式)。
为Mn),该化合物的化学式为________,Se的配位数为______,Mn和Se的摩尔质量分别为M1g/mol、M2g/mol,该晶体的密度为ρg/cm3,则Mn—Se键的键长为_____________nm(计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.实验室常用MnO2与浓盐酸反应制备Cl2(装置如图所示)。

(1)制备实验开始时,先检査装置气密性,接下来的操作依次是:_______(填序号)。
①往烧瓶中加入MnO2粉末;②加热;③往烧瓶中加入浓盐酸
(2)写出圆底烧瓶中发生反应的离子方程式_______________________。
(3)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度。甲同学提出下列具体方案。请你从下列实验方案中选择合理的实验方法_______(填字母序号)。
a.将Cl-转化为AgCl沉淀,过滤,洗涤,干燥,称量沉淀的质量
b.与足量NaHCO3固体反应,将反应后气体直接用碱石灰吸收,测定生成气体的质量
c.与足量锌反应,测量生成气体标准状况下的体积
II.为测定某亚硫酸钠样品纯度,研究小组利用如下装置(装置图中夹持仪器已省略)进行实验。
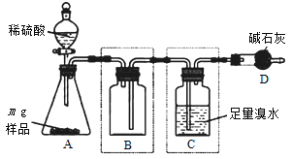
反应完全后,向C中溶液加入过量BaCl2溶液,过滤、操作①、干燥、称量,利用所得数据计算样品纯度。请回答:
(4)操作①的名称是____________。
(5)装置B的作用是______________________。
(6)最终所得固体质量为b g,则该样品中亚硫酸钠的质量分数为____________(用含字母m、b的代数式表示)。
(7)上述实验测得的样品纯度比实际偏低,为提高测定结果的准确度,可采取的改进措施是________________________________________(写一种)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com