
【题目】气体的体积主要由以下什么因素决定:( )
①气体的分子多少 ②气体分子的大小
③气体分子间的平均距离 ④气体分子的相对分子质量.
A. ①②B. ①③C. ②③D. ②④
 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】已知:Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,能氧化浓HCl生成Cl2;PbO2不稳定,随温度升高按下列顺序逐步分PbO2→Pb2O3→Pb3O4→PbO.现将a mol PbO2加热分解,收集产生的O2;向加热后所得固体中加入足量的浓盐酸,收集产生的Cl2 . 加热反应后所得固体中,Pb2+占Pb元素的物质的量分数为x;两步反应中收集的O2和Cl2的物质的量之和为y mol.试回答下列问题:
(1)试写出Pb2O3与浓盐酸反应的化学方程式 .
(2)用含x与a的表达式表示产生的O2、Cl2的物质的量n(O2)= , n(Cl2)= .
(3)写出y与a、x的函数关系式: .
(4)若两步反应中O2和Cl2的物质的量之比为5:3,则剩余固体中含有的物质为;其物质的量之比为 .
(5)PbO2和Pb经常作制造蓄电池的原材料,铅蓄电池的工作原理:Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O.现有一种生产NH4NO3的新工艺,电解NO制备NH4NO3 , 其工作原理如图所示,为使电解产物全部转化为NH4NO3 , 需补充物质A,A是 , 说明理由: . 生产1吨硝酸铵需消耗Pb的物质的量是kg(保留到整数).
2PbSO4+2H2O.现有一种生产NH4NO3的新工艺,电解NO制备NH4NO3 , 其工作原理如图所示,为使电解产物全部转化为NH4NO3 , 需补充物质A,A是 , 说明理由: . 生产1吨硝酸铵需消耗Pb的物质的量是kg(保留到整数).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置,则下列说法正确的是( ) 
A.图中甲池为原电池装置,Cu电极发生还原反应
B.实验过程中,甲池左侧烧杯中NO ![]() 的浓度不变
的浓度不变
C.若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是足量AgNO3溶液
D.若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.NA代表阿伏加德罗常数,1molC4H10中含共价键数目为14NA
B.某反应的△H=﹣88kJ?mol﹣1 , 则正反应活化能一定小于88kJ?mol﹣1
C.已知某温度下,Kw=l×10﹣13 , 若将pH=8的NaOH溶液与pH=5的H2SO4溶液混合保持温度不变,欲使混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为11:9
D.将浓度为0.1 mol?L﹣1 HF溶液加水不断稀释过程中,电离度和Ka(HF)保持不变, ![]() 始终保持增大
始终保持增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
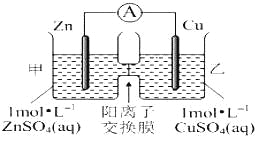
A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池的C(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阳离子通过交换膜向正极移动,阴离子通过交换膜向负极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解结晶水合物CuCl·2H2O制备CuCl,并进行相关探究。
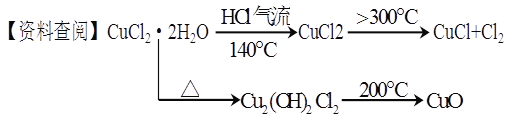
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是 。
(2)实验操作的先后顺序是![]()
![]() (填操作的编号)。
(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 。
(4)装置D中发生的氧化还原反应的离子方程式是 。
【探究反思】
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是 。
②若杂质是CuO,则产生的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各选项有机物数目,与分子式为ClC4H7O2且能与碳酸氢钠反应生成气体的有机物数目相同的是(不含立体异构)( )
A.分子式为C5H10的烯烃
B.分子式为C4H8O2的酯
C.甲苯( ![]() )的一氯代物
)的一氯代物
D.立体烷( ![]() )的二氯代物
)的二氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 直径介于1~100 nm之间的粒子称为胶体
B. 通过观察外观的方法可以区别胶体和溶液
C. 利用丁达尔效应可以区别溶液与胶体
D. 胶体区别于其他分散系的本质特征是丁达尔效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com