
【题目】二甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效,具有优良的环保性能。
请填写下列空白:
(l)与二甲醚相对分子质量相等且元素种类相同的有机物的结构简式是:_____________。
(2)二甲醚可由合成气(CO+H2)在一定条件下制得。用合成气制二甲醚时,还产生了一种可参与大气循环的无机化合物,该反应的化学方程式可能是:______________________________。
(3)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是:_________________________。
【答案】(1)CH3CH2OH、HCOOH
(2)3CO+3H2![]() CH3OCH3+CO2或2CO+4H2
CH3OCH3+CO2或2CO+4H2![]() CH3OCH3+H2O
CH3OCH3+H2O
(3)CH3OCH3+16OH--12e-=2CO32-+11H2O
【解析】
试题分析:(1)二甲醚分子式是C2H6O,与二甲醚相对分子质量相等且元素种类相同、分子式也相同的有机物为乙醇,其结构简式为C2H5OH;若相对分子质量相等且元素种类相同,分子式不同,则物质是甲酸,结构简式是HCOOH;(2)CO+H2在一定条件下合成二甲醚,可能生成二氧化碳或水,反应为3CO+3H2![]() CH3OCH3+CO2或2CO+4H2
CH3OCH3+CO2或2CO+4H2![]() CH3OCH3+H2O;(3)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。通入二甲醚的电极为负极,在负极上二甲醚失去电子,在碱性电解质中反应变为CO32-,该电池中负极上的电极反应式为CH3OCH3+16OH--12e-=2CO32-+11H2O;在正极上氧气获得电子变为OH-,电极反应式是O2+4e-+2H2O=4OH-。
CH3OCH3+H2O;(3)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。通入二甲醚的电极为负极,在负极上二甲醚失去电子,在碱性电解质中反应变为CO32-,该电池中负极上的电极反应式为CH3OCH3+16OH--12e-=2CO32-+11H2O;在正极上氧气获得电子变为OH-,电极反应式是O2+4e-+2H2O=4OH-。


科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
【实验I】制备NaNO2
该小组查阅资料知:①2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3
②NO能被酸性高锰酸钾氧化为NO3-。
设计制备装置如下(夹持装置略去)。

(1)装置A中用于盛放稀HNO3溶液的仪器名称为___________________;
写出装置A中发生主要反应的离子方程式 。
(2)装置D的作用为_________________。
(3)如果没有B装置,写出C中发生副反应的化学方程式①_______________、②____________。
(4)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。请设计一种提高NaNO2纯度的改进措施 。
【实脸II】测定制取的样品中NaNO2的含量
步骤:已知在酸性溶液中,NO2-可将MnO4-还原为Mn2+。为测定亚硝酸钠的含量,称取4.000 g样品溶于水配成250 mL溶液,取25.00 mL溶液于锥形瓶中,用0.1000 mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:

(5)根据表中数据,计算所得固体中亚硝酸钠的质量分数__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2mol A和2mol B两种气体相混合于体积为2L的某密闭容器中(容积不变),发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),2min末反应达到平衡状态(温度不变),生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态(温度不变),生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)X的值等于__________;
(2)A的转化率为_________________。
(3)生成D的反应速率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的非金属元素及化合物的特征性质有着重要的应用,请按要求回答:
(1)C、N、O、Si、S、Cl等元素形成的单质中
①属于空气主要成分它们相互反应的化学方程式_____________________;
②常用于自来水消毒的是实验室制备该气体的化学方程式_____________________。
(2)在CO、CO2、SO2、NO、NO2、SiO2等氧化物中:
①其中属于酸性氧化物的是______________,能形成酸雨的是_____________。
②光导纤维的主要成分与烧碱反应的化学方程式为___________________。
(3)在浓(稀)硝酸、浓(稀)硫酸中:
①常温下能使Fe、Al钝化的是_________。
②见光易分解的反应的化学方程式是:_____________________。
(4)在H2O2、NH3、HCl中:
①被称作绿色氧化剂,它与FeSO4酸性溶液反应的离子方程式为_______________________。
②可用于制氮肥、纯碱,加热条件下与氧气反应的化学方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池和电解池的比较中正确的是
A.能量转化形式相同
B.两极的名称相同
C.负极和阴极上移向的离子类别相同
D.负极和阳极上发生的反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关材料分类不正确的是
A.玻璃、水泥、陶瓷属于传统的无机非金属材料
B.聚氯乙烯属于有机材料
C.光导纤维属于新型无机非金属材料
D.玻璃钢属于金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
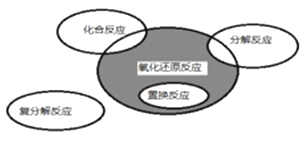
【题目】氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是
A. CuSO4+Mg=Cu+MgSO4
B. 2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C. 2Na2O2+2CO2===2Na2CO3+O2
D. 4Fe(OH)2+O2+2H2O===4Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关LiFePO4的说法中正确的是( )
A.LiFePO4是共价化合物
B.LiFePO4中所有元素都属于短周期元素
C.LiFePO4中的四种元素中有三种元素属于主族元素
D.Li和O2反应可生成既含有离子键又含有非极性键的Li2O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com