
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强(提示:Na2S +2HCl = 2NaCl+ H2S↑),某化学实验小组设计了如下实验,请回答下列问题:
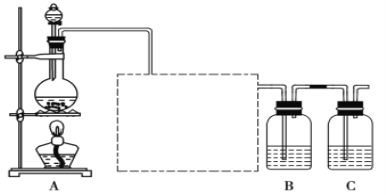
(1)画出虚线框内的实验装置图____,所加试剂为___________,该装置的作用是__________。
(2)装置B中盛放的试剂是____(填序号),
A.Na2S溶液B.Na2SO3溶液C.Na2SO4溶液
B装置中发生反应的离子方程式为___________________________。
(3)已知:①硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。②高氯酸的酸性比硫酸强;③铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;④HCl比H2S稳定;⑤硫酸比次氯酸稳定;能说明氯的非金属性比硫强的是____(填序号)。
A.全部 B. ①②③④ C.①②④⑤ D. ①③④⑤
(4)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:_____________________。
【答案】 饱和食盐水 除去Cl2中的HCl气体 A S2-+Cl2 = 2Cl-+S↓ B Cl2+2OH- = Cl-+ClO-+H2O
饱和食盐水 除去Cl2中的HCl气体 A S2-+Cl2 = 2Cl-+S↓ B Cl2+2OH- = Cl-+ClO-+H2O
【解析】
(1)氯气在饱和食盐水中溶解度很小,HCl易溶于水;
(2)从置换反应判断元素非金属性强弱分析,氯气能把硫元素从其硫化钠溶液中置换出来;
(3)依据元素周期律作答;
(4)氯气为有毒气体,要进行尾气处理。
(1)由于用浓盐酸制取氯气,且需要加热,即实验过程中要挥发出HCl气体,因此虚线框部分应是除去HCl气体的装置,可以使用洗气瓶,瓶内盛装饱和食盐水,既除去HCl,又降低氯气在水中的溶解度,所用装置为: ;所加试剂为饱和食盐水;装置的作用为:除去Cl2中的HCl气体;
;所加试剂为饱和食盐水;装置的作用为:除去Cl2中的HCl气体;
(2)要在B中发生氯气置换出硫的反应,结合已知信息在给定试剂中只能选取Na2S溶液,故A项正确;发生的是置换反应,其离子方程式为:S2-+Cl2 = 2Cl-+S↓;
(3)①硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子,则氯原子得电子能力强,即非金属性较硫强,①项正确;
②最高价氧化物对应水化物的酸的酸性越强,则元素非金属性越强,②项正确;
③单质将同样的金属氧化到的价态越高则原子的得电子能力强,③项正确;
④元素的氢化物的稳定性越强则原子的得电子能力越强,④项正确;
⑤硫酸比次氯酸稳定,不能说明非金属性强弱,⑤项错误;
综上所述,①②③④项正确,答案选B。
(4)实验时,用氢氧化钠对氯气进行尾气处理,反应的原理方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】下表中物质的分类全部正确的一组是
单质 | 氧化物 | 盐 | 混合物 | |
A | 臭氧 | 氯化氢 | 小苏打 | 漂白粉 |
B | 水银 | 氧化钠 | 纯碱 | 生理盐水 |
C | 溴水 | 水 | 硫酸钡 | 空气 |
D | 硫粉 | 干冰 | 氯化铵 | 冰水混合物 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯酚经下列反应可制香料M和高分子化合物N(部分产物及反应条件已略去)
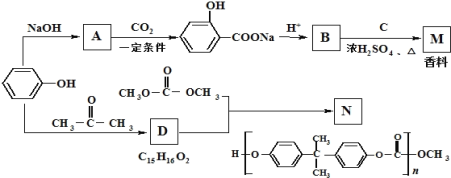
(1)已知C的分子式为C5H12O,C能与金属Na反应,C的一氯代物有2种,则C的结构简式为 ________.
(2)由D生成N的反应类型是_________.
(3)由苯酚生成D的化学方程式是_________.
(4)F是分子量比B大14的同系物,则F的分子式是__________________ .F有多种同分异构体,符合下列条件的F的同分异构体有_______ 种
①遇FeCl3溶液显紫色,且能水解②苯环上有两个取代基,且苯环上的一溴代物只有两种。
(5)已知: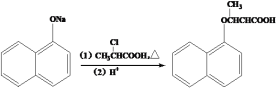 ,写出以苯酚、乙醇和CH2ClCOOH为原料制备
,写出以苯酚、乙醇和CH2ClCOOH为原料制备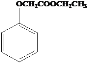 的合成路线流程图(无机试剂任用)_________。
的合成路线流程图(无机试剂任用)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸的物质的量浓度为______molL-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400molL-1的稀盐酸。
①该学生需要量取______mL上述浓盐酸进行配制。
②所需的实验仪器有:胶头滴管、烧杯、量筒、玻璃棒,配制稀盐酸时,还缺少的仪器有_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
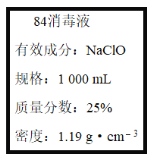
(1)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=____mol·L-1。
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是____(填字母)。
a.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
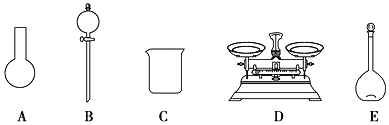
b.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
c.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
d.需要称量NaClO固体的质量为143.0 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA为阿伏加德罗常数,则下列叙述正确的是
A. 标准状况下,12 g C60中含有的碳原子数为NA
B. 3.9 g金属钾变为钾离子时,失去的电子数为NA
C. 标准状况下,22.4 L以任意比例混合的CO2与CO气体中含有的碳原子数约为2NA
D. 在1 L 1 mol·L-1的盐酸中,所含氢原子数约为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、CO、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ/mol
N2(g) + 2O2(g)= 2NO2(g) △H= +133 kJ/mol
H2O(g) =H2O(l) △H= -44 kJ/mol
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为_____________。
Ⅱ.脱碳:
(2)向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应 CO2(g) + 3H2(g) ![]() CH3OH(l) + H2O(l)。下列叙述能说明此反应达到平衡状态的是__________。
CH3OH(l) + H2O(l)。下列叙述能说明此反应达到平衡状态的是__________。
A.混合气体的平均式量保持不变 B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等 D.混合气体的密度保持不变
E.1 mol CO2生成的同时有3 mol H—H键断裂
(3)在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,发生反应CO(g) + 2H2(g) ![]() CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图所示。
CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图所示。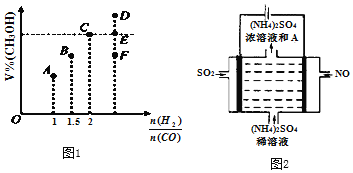
①当起始n(H2)/n(CO)=2,经过5min达到平衡,CO的转化率为0.4,则0~5min内平均反应速率V(H2)=___________。若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将__________(选填“增大”、“减小”或“不变”);
②当起始n(H2)/n(CO)=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的_________点(选填“D”、“E”或“F”)
Ⅲ.脱硫:
(4)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为_______,阴极的电极反应式是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com