
【题目】某溶液中可能含有Na+、Mg2+、Fe2+、H+、HCO3-、OH-、Cl-、NO3-、I-中的若干种,向该溶液中加入铝粉后,溶液中有AlO2-生成,则原溶液中能大最共存的离子最多有
A. 4种 B. 5种 C. 6种 D. 7种
科目:高中化学 来源: 题型:
【题目】铝热反应是铝的一个重要性质。


(1)按如图装置进行实验,可观察到反应剧烈,火星四射,漏斗下方有红热熔融物“铁块”流出。
该反应的化学方程式为_____,其能量变化为如图中的______(填“A”或“B”)所示。

(2)某校化学兴趣小组同学,为了测定铝热反应后得到“铁块”混合物中铝的含量。取“铁块”样品研碎称得质量为x g,加入如图装置,再滴入足量NaOH溶液充分反应,测量生成气体体积为a ml(标况)。
①仪器A的名称为_______。
②写出样品中Al与NaOH反应的化学方程式_______。
③该小组同学改进实验,用恒压漏斗(如图)代替仪器A,其优点有________(写2点)。
④该样品中铝的含量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸为弱酸,其钠盐(亚硝酸钠NaNO2)外观酷似食盐且有咸味,过量使用会使人中毒。其银盐不溶于水。某化学兴趣小组对亚硝酸钠的制备进行了探究。
(1)请设计一种简单方法鉴别NaCl和NaNO2 :___________。
(2)利用如图完成一氧化氮与过氧化钠反应制备业硝酸钠。查阅资料:2NO + Na2O2 =2NaNO2, 2NO2+ Na2O2=2NaNO3, NO 能被酸性高锰酸钾氧化为NO3-。回答下列问题:

① 检查装置气密性后,应进行的操作是_________。
② 装置B 中Cu 参与反应的离子方程式为______,装置C 的作用是______。
③ 装置E发生反应的离子方程式为________。
④ 同学们经过讨论认为上述装置仍然存在缺陷,D中生成的产物不纯,D管中可能含有的杂质为________(填化学式),你认为应该进行的改进是__________。
(3)测定制取样品中NaNO2的纯度。
步骤:a.在5个有编号的带刻度的试管中分别加入不同体积、相同浓度的NaNO2溶液,各加入1mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10mL,并振荡,制成标准色阶;
试管编号 | ① | ② | ③ | ④ | ⑤ |
NaNO2含量(mg/L) | 0 | 20 | 40 | 60 | 80 |
b.称量0.10g制得的样品,溶于水配成500mL溶液。取5mL待测液,加入1mLM,再加入蒸馏水至l0mL,并振荡,与标准色阶比较。
比较结果:待测液与④标准色阶相同,则制取样品中NaNO2的纯度是________。
查阅资料可知:维生素C可有效降低NaNO2的含量。请完成下列实验验证方案:取5 mL 待测液,加入______,振荡,再加入1mL M溶液,_____,再振荡,与④ 标准色阶对比。实验现象为紫红色比④ 标准色阶浅,则证明维生素C可以有效降低NaNO2的含量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g) ![]() 2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的表示,正确的是( )
2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的表示,正确的是( )
A. 用A表示的反应速率是0.4 mol/(L·min)
B. 可以用B、C、D表示反应的速率,且数值相同
C. 在2 min末的反应速率,用B表示是0.3 mol/(L·min)
D. 在这2 min内用B和C表示的反应速率的值都是逐渐减小的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.碳酸钙与醋酸反应:CaCO3+2H+=Ca2++H2O+CO2↑
B.铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+
C.碳酸氢钠溶液与氢氧化钠溶液混合:HCO3-+OH-=H2O+CO2↑
D.将氯气通入KBr溶液中:Cl2+2Br-=2Cl-+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机高分子化合物M的一种合成路线如下:

已知:I.RCHBr-CH2Br![]() RC≡CH;
RC≡CH;
II.CH≡CH+CH2=CH-CH=CH2![]()
![]()
Ⅲ.  。
。
请回答下列问题:
(1)A的化学名称为______,F中所含官能团的名称为_________。
(2)C+D→E的反应类型为__________。
(3)B的结构简式为______,C的分子中最多有_____个原子在同一直线上。
(4)H+I→M的化学方程式为______________。
(5)在催化剂,加热条件下,G与氧气反应生成Q(C9H8O3),同时满足下列条件的Q的同分异构体有_____种(不考虑立体异构),其中核磁共振氢谱有6 组吸收峰的结构简式为_________。
①除苯环外不含其他环状结构;②能与FeCl3溶液发生显色反应;③能与NaHCO3溶液反应生成CO2
(6)参照上述合成路线和相关信息,以甲醇和一氯环己烷为有机原料(无机试剂任选),设计制备己二酸二甲酯的合成路线:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属与水的反应说法正确的是
A. 钠可以沉入水底与水剧烈反应
B. 由于铝锅可以用于烧水,因此铝不能跟沸水反应
C. 铁和冷水可以反应生成四氧化三铁和氢气
D. 金属的活泼性越弱,与水反应时需要的条件越苛刻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法处理酸性污水的工作原理如图。下列说法正确的是
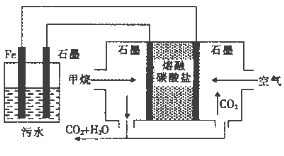
A. 左侧装置中的铁电极可换成石墨电极
B. 通入甲烷的石墨电极的电极反应式为: CH4+4CO32——8e—=5CO2+2H2O
C. 通入空气的石墨电极做正极,发生氧化反应
D. 若左侧装置中石墨电极产生标况下气体44.8L气体, 则消耗2mol甲烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com