
| A. | 纯碱溶液去油污 | B. | 明矾可作净水剂 | ||
| C. | 加热氯化铁溶液颜色变深 | D. | 硫酸氢钠溶液显酸性 |
分析 A、油脂属于酯类,在碱性条件下发生水解;
B、明矾溶于水后能水解出氢氧化铝胶体;
C、盐类的水解吸热;
D、NaHSO4是强酸强碱盐.
解答 解:A、纯碱为Na2CO3,在溶液中水解显碱性,而油脂属于酯类,在碱性条件下发生水解,故纯碱能去油污,故A错误;
B、明矾溶于水后能水解出氢氧化铝胶体,具有吸附功能,故能去油污,故B错误;
C、盐类的水解吸热,故加热氯化铁溶液后,对氯化铁的水解有促进作用,能水解出氢氧化铁胶体显红褐色,故颜色变深,故C错误;
D、NaHSO4是强酸强碱盐,不能水解只能电离:NaHSO4=Na++H++SO42-,故与水解无关,故D正确.
故选D.
点评 本题考查了盐类水解的应用,难度不大,应注意的是明矾净水、氢氧化铁胶体的制备和纯碱去油污均为盐类水解的应用.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| B. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═2HClO+SO32- | |
| C. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放射元素 | B. | ⅦA族元素 | C. | 卤化银 | D. | ⅠA族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | W |
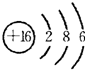 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
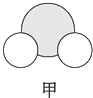 | 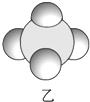 |  |
| 是地球上最常见的物质之一,常温为液态,是包括人类在内所有生命生存的重要资源,也是生物体最重要的组成部分 | 无色,无味且易燃,是21世纪的主要能源 | 弱酸,有强氧化性,可以用于消毒杀菌 |
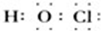 ,丙与SO2水溶液可发生氧化还原反应,生成两种强酸,化学反应方程式为HClO+H2O+SO2=H2SO4+HCl.
,丙与SO2水溶液可发生氧化还原反应,生成两种强酸,化学反应方程式为HClO+H2O+SO2=H2SO4+HCl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
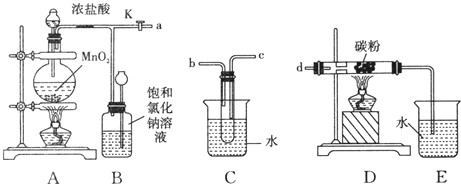
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只能是酸 | B. | 只能是碱 | ||
| C. | 可能是酸也可能是碱 | D. | 只能是盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 mL 0.1 mol•L-1的AlCl3溶液 | B. | 20 mL 0.1 mol•L-1的CaCl2溶液 | ||
| C. | 30 mL 0.2 mol•L-1的KCl溶液 | D. | 100 mL 0.25 mol•L-1的NaCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com