
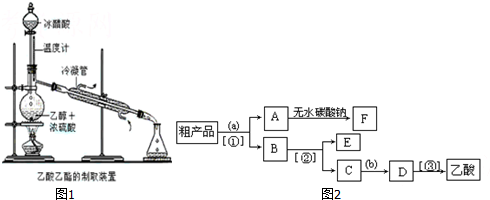
分析 (1)加入碎瓷片可防止液体暴沸;
(2)从防止酸液飞溅的角度分析;
(3)反应为可逆反应,不能完全进行;
(4)粗产品乙酸乙酯中含有乙酸与乙醇,用饱和的碳酸钠溶液反应掉乙酸,溶解乙醇,同时降低乙酸乙酯的溶解度,便于溶液分层,乙酸乙酯密度比水小,乙酸乙酯在上层,然后利用分液,乙酸乙酯加入无水碳酸钠吸收其中的水,可得乙酸乙酯;溶液中含有乙醇、碳酸钠、乙酸钠,进行蒸馏可以收集乙醇,向蒸出乙醇的溶液中加入硫酸,可以得到乙酸,再进行蒸馏可以收集乙酸.
解答 解:(1)加入碎瓷片可防止液体暴沸,故答案为:防止液体暴沸;
(2)浓硫酸溶于水放出大量的热,且密度比水大,为防止酸液飞溅,应先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡,
故答案为:乙醇;浓硫酸;
(3)乙酸和乙醇制备乙酸乙酯的反应为可逆反应,反应不能进行到底;乙醇、乙酸受热挥发原料损失,
故答案为:该反应是可逆反应,反应不能进行到底;乙醇、乙酸受热挥发原料损失;
(4)粗产品乙酸乙酯中含有乙酸与乙醇,用饱和的碳酸钠溶液反应掉乙酸,溶解乙醇,同时降低乙酸乙酯的溶解度,便于溶液分层,乙酸乙酯密度比水小,乙酸乙酯在上层,然后利用分液,乙酸乙酯加入无水碳酸钠吸收其中的水,可得乙酸乙酯;溶液中含有乙醇、碳酸钠、乙酸钠,进行蒸馏可以收集乙醇,向蒸出乙醇的溶液中加入硫酸,可以得到乙酸,再进行蒸馏可以收集乙酸;
故答案为:饱和的碳酸钠溶液;硫酸;分液,蒸馏,蒸馏.
点评 本题考查乙酸乙酯的制备,难度不大,注意实验混合液的配制、饱和碳酸钠溶液的作用以及酯化反应的机理,(4)中试剂b选择,由于盐酸易挥发,不能使用盐酸.


科目:高中化学 来源: 题型:选择题
| A. | NH3、HD、C3H8 | B. | PCl3、CO2、H2SO4 | C. | SO2、BN、P2O5 | D. | CCl4、Na2S、H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
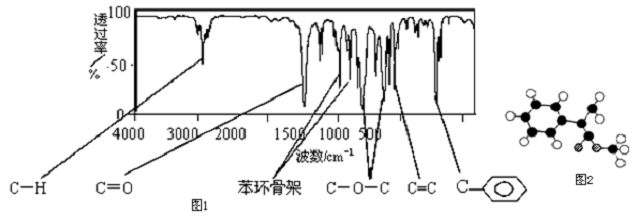
 (包括顺反异构)
(包括顺反异构)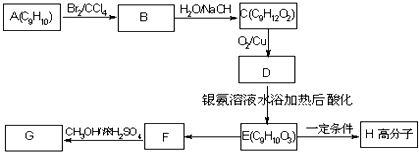
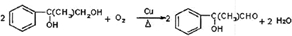
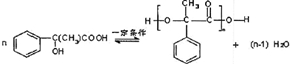
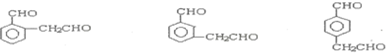 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
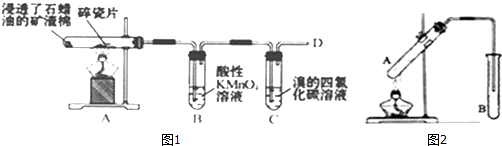
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| ① | 2 | 20 | |
| ② | 2 | 20 | 10滴饱和MnSO4溶液 |
| ③ | 2 | 30 | |
| ④ | 1 | 30 | 1mL蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4可以写成FeO•Fe2O3,Pb3O4也可以写成PbO•Pb2O3 | |
| B. | 不能用电解AlCl3溶液来制取金属铝,也不能用电解MgCl2溶液来制取金属镁 | |
| C. | Fe和S直接化合不能得到Fe2S3,Al和S直接化合也不能得到Al2S3 | |
| D. | FeS可以和稀硫酸反应制取硫化氢气体,CuS也可以和稀硫酸反应制取硫化氢气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(苯酚):加浓溴水振荡,分液 | |
| B. | 硝酸(硝酸镁):加热,蒸馏 | |
| C. | 肥皂液(甘油):加食盐颗粒,过滤 | |
| D. | 乙酸乙酯(乙酸):加氢氧化钠溶液,分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com