
【题目】室温下,将1 mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1 mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)![]() CuSO4(s)+5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4(s)+5H2O(l),热效应为ΔH3。则下列判断正确的是
A.ΔH2>ΔH3 B.ΔH1<ΔH3 C.ΔH1+ΔH3=ΔH2 D.ΔH1+ΔH2>ΔH3
科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化还原反应同时又是吸热反应的是()
A. Ba(OH)2·8H2O与NH4Cl反应
B. 铝与稀盐酸
C. 灼热的炭与水蒸气生成一氧化碳和氢气的反应
D. 煤与O2的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能说明氯原子得电子能力比硫原子强的是
①HC1的溶解度比H2S大
②HC1的酸性比H2S强
③HCl的稳定性比H2S强
④HC1的还原性比H2S强
⑤HC1O的酸性比H2SO4强
A. ①②⑤ B. ③④ C. ③ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g)![]() 2C1NO(g)。
2C1NO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①2NO2(g)+NaC1(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaC1(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+C12(g)![]() 2C1NO(g) K3
2C1NO(g) K3
则K1,K2,K3之间的关系为K3=______________。
(2)已知几种化学键的键能数据如下表(亚硝酸氯的结构为Cl-N=O):

则2NO(g)+C12(g)![]() 2C1NO(g)反应的ΔH和a的关系为ΔH =_____________kJ/mol。
2C1NO(g)反应的ΔH和a的关系为ΔH =_____________kJ/mol。
(3)300℃时,2NO(g)+C12(g)![]() 2ClNO(g)的正反应速率表达式为v正 = k·cn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正 = k·cn(ClNO),测得速率和浓度的关系如下表:
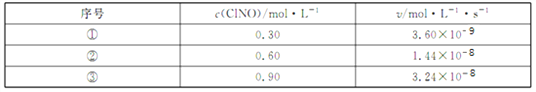
n =____________;k =__________________(注明单位)。
(4)在1L的恒容密闭容器中充入2molNO(g)和1molC12(g),在不同温度下测得c(C1NO)与时间的关系如图A:

①该反应的ΔH ____________0(填“>”、“<”或“=”);
②反应开始到10min时NO的平均反应速率v(NO)=____________mol/(L·min);
③T2时该反应的平衡常数K=____________。
(5)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是____________点,当n(NO)/n(C12)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的____________点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物与生产生活关系密切。请完成下列填空:
(1)肼由N、H两种元素组成,它常用作火箭推进剂。肼的相对分子质量为32,分子中N、H原子的个数比为1:2。肼的分子式为_________。1mol的肼分子中含有的电子总数为_____NA(NA为阿伏伽德罗常数的值)。16g肼分子中所含的氮原子数与标准状况下____L N2中所含的氮原子数相等。
(2)在相同温度和压强下,体积相同的两个容器中分别盛有N2和O2。下列说法不正确的是____(填序号)。
A.N2和O2的密度之比为7:8 B.两容器内的气体具有相同的分子数
C.两容器内的气体具有相同的原子数 D.两容器内的气体具有相同的质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质与其用途相符合的是
①Cl2——自来水消毒剂 ②浓硫酸——干燥剂 ③AgI——人工降雨
④FeCl3——印刷电路板 ⑤淀粉——检验I2的存在 ⑥Na2O2——漂白纺织物
A. ②③④⑤⑥ B. ①②③④⑤ C. ②③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1 mol L-1的Na0H溶液分别滴定体积均为20mL、浓度均为0.1 mol L-1的HCl溶液和HX溶液,溶液的pH随加入 Na0H溶液体积的变化如图所示。下列说法正确的是( )

A. M点对应溶液中:c(HX)<C(X-)
B. HX的电离平衡常数Ka约为1×10-5
C. P 点对应溶液中 c(Cl-) = 0.05 mol L-1
D. N点对应溶液pH>7的原因是X-+H20![]() HX+0H-
HX+0H-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种常见的非金属单质,B是氧化物,E是A的氢化物,D是A的最高价氧化物对应的水化物,上述物质间转化关系如图所示。下列说法错误的是 ( )

A. 若E、D的水溶液均呈酸性,则A为硫
B. 若D是一种难溶于水的物质,则A为硅
C. 若E、D的水溶液均呈酸性,则B能与水反应
D. 若D是一种难溶于水的物质,则B能与水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在水电离出的c(H+)=10-14mol/L的溶液中,一定能大量共存的( )
A.K+、Na+、HCO3-、Cl-B.K+、Br-、AlO2-、Cl-
C.SO42-、Na+、NO3-、Cl-D.SO42-、NH4+、Al3+、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com