
 过氧化钠可做航天飞船的供氧剂,对其纯度要求很高,某小组同学为了测定过氧化钠的纯度(杂质为碳酸钠),设计了如下方案:
过氧化钠可做航天飞船的供氧剂,对其纯度要求很高,某小组同学为了测定过氧化钠的纯度(杂质为碳酸钠),设计了如下方案:| 氢氧化钠浓度(mol•L-1) | 5 | 2 | 1 | 0.01 |
| 变红后褪色的时间(s) | 8 | 94 | 450 | 长时间不褪色 |
分析 (1)反应中会生成微弱的氢氧化钙,导致测定碳酸钙测定质量偏大;
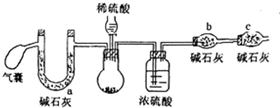
(2)圆底烧瓶中生成二氧化碳,用浓硫酸干燥二氧化硫,干燥管b中碱石灰吸收二氧化碳,根据干燥管b质量增大可知二氧化碳的质量,进而计算样品中碳酸钠的质量,可得过氧化钠的纯度,干燥管c吸收空气中水蒸气与二氧化碳,防止加入b中,开始利用气囊鼓入空气排尽装置中空气,用a装置吸收鼓入空气中二氧化碳与水蒸气,结束后再排出装置中二氧化碳进入b中被完全吸收;
若利用与水代替稀硫酸,挥发出的HCl会被b中碱石灰吸收,测定二氧化碳的质量偏大;
(3)滴定终点落在指示剂的变色范围之内,终点时溶液用颜色由黄色变为橙红色;计算消耗HCl的物质的量,反应生成NaCl,根据离子守恒可知过氧化钠、碳酸钠中钠离子总物质的量,再结合质量列方程计算;
(4)由表中数据可知,酚酞在浓的NaOH溶液中先变红后褪色,且碱浓度越大、褪色越快;
若由于生成过氧化氢使溶液红色褪去,可以加入二氧化锰使之分解,再加入酚酞溶液,与直接加入酚酞溶液进行对比验证.
解答 解:(1)反应中会生成微弱的氢氧化钙,导致测定碳酸钙测定质量偏大,计算得到碳酸钠的质量偏大,故测得的过氧化钠的纯度比实际的偏低,
故答案为:生成微溶的Ca(OH)2,致使m2数值偏大;
(2)圆底烧瓶中生成二氧化碳,用浓硫酸干燥二氧化硫,干燥管b中碱石灰吸收二氧化碳,根据干燥管b质量增大可知二氧化碳的质量,进而计算样品中碳酸钠的质量,可得过氧化钠的纯度,干燥管c吸收空气中水蒸气与二氧化碳,防止加入b中,开始利用气囊鼓入空气排尽装置中空气,用a装置吸收鼓入空气中二氧化碳与水蒸气,结束后再排出装置中二氧化碳进入b中被完全吸收;
若利用与水代替稀硫酸,挥发出的HCl会被b中碱石灰吸收,测定二氧化碳的质量偏大,计算碳酸钠的质量偏大,故沉淀过氧化钠的纯度偏低,
故答案为:排出装置中生成的CO2完全被碱石灰吸收;防止空气中水和二氧化碳进入b中;低;
(3)滴定终点落在指示剂的变色范围之内,终点时溶液由黄色变成橙色,且半分钟内不变黄,
消耗HCl的物质的量为0.001V L×c mol/L=0.001Vc mol,则生成NaCl为0.001Vc mol,
设过氧化钠、碳酸钠物质的量分别为xmol、ymol,则:
由钠离子守恒:2x+2y=0.001Vc
根据二者总质量:78x+106y=m1
解得x=$\frac{0.053Vc-{m}_{1}}{28}$,
则过氧化钠的含量为$\frac{\frac{0.053Vc-{m}_{1}}{28}mol×78g/mol}{{m}_{1}}$×100%=$\frac{39(0.053Vc-{m}_{1})}{14{m}_{1}}$×100%,
故答案为:溶液由黄色变成橙色,且半分钟内不变黄;$\frac{39(0.053Vc-{m}_{1})}{14{m}_{1}}$×100%;
(4)由表中数据可知,酚酞在浓的NaOH溶液中先变红后褪色,且碱浓度越大、褪色越快;
若由于生成过氧化氢使溶液红色褪去,可以加入二氧化锰使之分解,再加入酚酞溶液,与直接加入酚酞溶液进行对比验证,验证假设二的实验方案为:取两份等量的反应液于试管中,向其中一支试管加入少量二氧化锰并微热,滴几滴酚酞,溶液变红且不褪色,另一支试管中直接加入几滴酚酞,溶液变红后又褪色,说明假设二成立,
故答案为:酚酞在浓的NaOH溶液中先变红后褪色,且碱浓度越大、褪色越快;
取两份等量的反应液于试管中,向其中一支试管加入少量二氧化锰并微热,滴几滴酚酞,溶液变红且不褪色,另一支试管中直接加入几滴酚酞,溶液变红后又褪色,说明假设二成立.
点评 本题考查物质含量测定实验、物质性质探究实验及实验方案设计等,(3)中含量表达式为易错点,较好地考查学生对原理的理解与分析计算能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 次数 | 1 | 2 | 3 |
| 滴定体积/mL | 19.60 | 19.65 | 19.55 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 中药在世界医学界越来越受到关注.中药药剂砒霜(主要成分As2O3)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注.
中药在世界医学界越来越受到关注.中药药剂砒霜(主要成分As2O3)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注. ,则其在周期表中的位置是第四周期,VA族.
,则其在周期表中的位置是第四周期,VA族.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,它是极性(填“极性”或“非极性”)键形成的非极性分子.
,它是极性(填“极性”或“非极性”)键形成的非极性分子.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15 种 | B. | 16 种 | C. | 17 种 | D. | 18 种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com