
【题目】加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解,在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
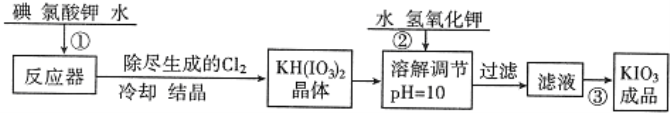
(1)已知步骤①反应器中发生的反应中,单质碘和氯酸钾的物质的量之比为6:11,反应器中发生的化学方程式为6I2+11KClO3+3H2O→6KH(IO3)2+5KCl+3Cl2↑。参照碘酸钾的溶解度:
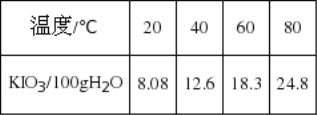
操作③得到碘酸钾晶体,方法是____________、____________:
(2)已知: KIO3+ 5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32—=2I—+S4O62—
检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应。用四氯化碳检验碘单质时,看到的明显现象有____________
(3)检验加碘食盐中碘的含量,学生乙设计的实验步骤如下:
①准确称取wg食盐,加适量蒸馏水使其完全溶解;
②用稀硫酸酸化所得食盐溶液,加入过量KI溶液充分混合;
③以淀粉为指示剂,逐滴加入2.0╳10—3mol/L的Na2S2O310.0mL,恰好反应完全。
则加碘食盐样品中的碘元素含量是_____ mg/kg (以含w 的代数式表示)。
(4)学生丙又对纯净的NaCl进行了下列实验:

请推测实验中产生蓝色现象的可能原因____________,用化学方程式表示。
(5)根据学生丙的实验结果,学生乙测得的食盐中碘元素的含量可能____________ (填“偏高”、“偏低"或“准确")。原因是____________
【答案】蒸发浓缩 降温结晶 下层四氯化碳呈紫色 ![]() 4 I—+4H+ +O2=2 I2+2H2O 偏高 过量的I—会被空气中的氧气氧化为I2
4 I—+4H+ +O2=2 I2+2H2O 偏高 过量的I—会被空气中的氧气氧化为I2
【解析】
(1)由KIO3溶液得到KIO3成品,则需要将溶剂蒸发掉,而得到浓缩的KIO3溶液,该操作为蒸发浓缩;为了防止形成的晶体KIO3受热分解,应停止加热,用仪器的余热蒸干溶剂,该操作叫作降温结晶;
(2)由于碘单质易溶于四氯化碳,所以用四氯化碳检验碘单质时,混合液分层,下层为四氯化碳层,由于萃取了碘单质,下层液体的颜色为紫红色;故答案为:液体分层,下层液体呈现紫红色;
(3)设碘酸钾的物质的量为x,根据反应KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O、I2+2S2O32-=2I-+S4O62-可得关系式:KIO3~3I2~6S2O32-,
则 KIO3~3I2~6S2O32-
1 6
x 2.0×10-3mol/L×0.01L
x=![]() =
=![]() ×10-5mol,根据碘原子守恒知,碘元素的质量=
×10-5mol,根据碘原子守恒知,碘元素的质量=![]() ×10-5mol×127g/mol=
×10-5mol×127g/mol=![]() ×10-5molg,所以碘元素的质量分数为:
×10-5molg,所以碘元素的质量分数为:![]() ×100%=
×100%=
![]() mg/kg,故答案为:
mg/kg,故答案为:![]() ;
;
(4)酸性条件下,碘离子被氧气氧化生成碘单质,离子反应方程式为:4I-+4H++O2=2I2+2H2O;且酸性条件下,过量的碘离子易被空气中氧气氧化生成碘单质,导致测定结果偏大,故答案为:4I-+4H++O2→2I2+2H2O;学生乙实验结果会偏大;过量的I-会被空气中的氧气氧化为I2。


科目:高中化学 来源: 题型:
【题目】在一定条件下,容积为2 L的密闭容器中,将2 mol L气体和3 mol M气体混合,发生如下反应:2L(g)+3M(g) ![]() xQ(g)+3R(g),10 s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
xQ(g)+3R(g),10 s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
(1)10 s末L的物质的量浓度为________。
(2)前10 s内用M表示的化学反应速率为________。
(3)化学方程式中x值为________。
(4)在恒温恒容条件下,往容器中加入1 mol氦气,反应速率________(填“增大”、“减小”或“不变”,下同)。
(5)在恒温恒压条件,往容器中加入1 mol氦气,反应速率________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为由石油制取汽油的装置示意图,根据图示回答下列问题。

(1)图中的两处明显的错误是________________、__________________
(2)A仪器的名称是________,B仪器的名称是________。
(3)实验时 A 中除加入石油外,还需加入少量__________,其作用是__________________。
(4)收集完汽油后,是先撤酒精灯还是先停冷凝水?
______________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Mg2+、Ba2+、CO32-,SO42-,现取三份100mL该溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.08mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤干燥后,沉淀质量为2.33g.
根据上述实验,以下推测正确的是
A.K+一定存在
B.100mL溶液中含0.01mol CO32-
C.Cl—一定存在
D.Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(密度为1.84g/cm3)配制100mL 1.0mol/L的稀硫酸,现给出下列仪器(配制过程中可能用到):
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)需量取浓硫酸的体积为________mL
(2)实验时选用的仪器有________
(3)配制过程中,下列情况会使配制结果偏高的是________ (填序号)
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
④量取浓硫酸时仰视量简刻度
⑤移液时未洗涤烧杯和玻璃棒
(4)在容量规使用方法中,下列操做不正确的是________ (填序号)
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶
D.将准确量取的18.4mol/L的硫酸,注入已盛有30mL水的100mL的容量瓶中,加水至刻度线
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的叙述中正确的是 ( )
A. pH=0的H2SO4溶液与1 mol·L-1 的Ba(OH)2溶液中水的电离程度相同
B. 0.2mol·L-1 CH3COOH溶液中的c(H+)是0.1mol·L-1 CH3COOH中的c(H+)的2倍
C. 室温时,pH=2的CH3COOH和0.01mol·L-1 NaOH溶液等体积混合,混合后pH=7
D. 等物质的量浓度的Na2S和NaHS的混合溶液中:2c(Na+)=3[c(S2-)+c(HS-)+c(H2S)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列有关说法正确的是
A. 60g冰醋酸晶体中,含阴离子数目为NA
B. 标准状况下,22.4LCCl4中含有分子的数目为NA
C. 常温下,46gNO2与N2O4混合气体中含分子数为NA
D. 32gCu投入300mL10mol/L的浓硝酸中,充分反应后转移电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
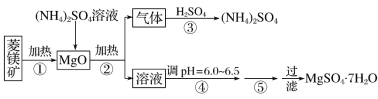
(1)步骤②中发生反应的离子方程式为__________________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是_______________________________________。
(3)步骤⑤的操作为________________________________________________________。
(4)若要除去MgSO4溶液中的FeSO4应先加________,再加入过量__________,过滤即可把杂质除尽;请用离子方程式以及文字说明除杂原理___________________________________
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____________(已知25 ℃时 ,Ksp[Mg(OH)2]=5.6×10-12 )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知钍![]() Th的原子可发生下列放射性变化:
Th的原子可发生下列放射性变化: ![]() Th→
Th→![]() X+
X+![]() He,生成的X是与Mg同主族的一种元素的原子,下列对X的推断错误的是
He,生成的X是与Mg同主族的一种元素的原子,下列对X的推断错误的是
A. X的氢氧化物是一种强碱B. X元素位于第六周期
C. X的碳酸盐难溶于水D. X的最高化合价为+2价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com