
| Cu |
| △ |
| KMnO4 |
| H+ |
| A |
| 浓H2SO4 |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、增重10% | B、增重30% |
| C、不变 | D、减轻20% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、其他条件不变情况下,增加A(g)的质量,则a(A)降低,a(B)升高 |
| B、其他条件不变情况下,增加压强,a(A)升高,则x>3 |
| C、其他条件不变情况下,升高温度,a(A)降低,则△H>0 |
| D、其他条件不变情况下,加入催化剂,则平衡右移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
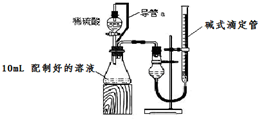 实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数w(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.
实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数w(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
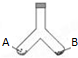 如图所示是一密闭容器,已知A端盛2.3g金属钠,B端盛有xgHgO,当同时加热容器的两侧支管时,钠着火燃烧,冷却后测得容器中空气成分并未发生变化,求x的值.(Hg的相对原子质量是200.6)
如图所示是一密闭容器,已知A端盛2.3g金属钠,B端盛有xgHgO,当同时加热容器的两侧支管时,钠着火燃烧,冷却后测得容器中空气成分并未发生变化,求x的值.(Hg的相对原子质量是200.6)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com