
【题目】氨是重要的无机化工产品之一,在国民经济中占有重要地位。我国采用铁触媒(以铁为主的混合物)做催化剂合成氨。回答下列问题:
(1)Fe基态原子核外电子排布式为____。氮化铁是一种重要的无机化合物,不溶于水,暴露在潮湿环境中可释放出氨气,元素Fe和N中,第一电离能较大的是_____,基态原子核外未成对电子数较多的是_______。
(2)N的氧化物有N2O等,N2O与CO2互为等电子体,N2O的空间构型为__________。
(3)N有多种氢化物,其中肼(N2H4)常用作火箭推进剂的燃料,N2H4中N原子的杂化形式为____。
(4)N、P、As为同族元素,NH3、PH3、AsH3三种物质的沸点由高到低的顺序为_____。原因是____。
(5)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中存在的化学键类型有_______。
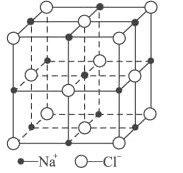
(6)FeO晶体的晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为428pm,则该晶体的密度为____g/cm3(列出计算式即可,用NA表示阿伏加德罗常数的值)。
 。
。
【答案】 1s22s22p63s23p63d64s2 N Fe 直线形 sp3 NH3﹥AsH3﹥PH3 NH3之间形成了氢键,分子间作用力大,所以沸点高,AsH3和PH3结构相似,而AsH3的相对分子质量更大,故其分子间作用力比PH3大,所以AsH3的沸点比PH3更高 离子键、配位键、共价键或(离子键、配位键、σ键、π键) ![]()
【解析】(1)铁的原子序数为26,根据能量最低原理其态原子的电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2;元素Fe和N中,N的其态原子的电子排布式为1s22s22p3,最外层电子受到核的吸引力大于铁,第一电离能较大的是N,根据二者的电子排布可知,基态原子核外未成对电子数分别为4和3,较多的是铁,故答案为:1s22s22p63s23p63d64s2;N;Fe;
(2)N2O与CO2互为等电子体,结构相似,因此N2O的空间构型为直线形,故答案为:直线形;
(3)N2H4中N原子与3个原子相连,含有1个孤电子对,价层电子对数=3+1=4,采用sp3杂化,故答案为:sp3;
(4)NH3分子间能够形成氢键,沸点最高,AsH3和PH3结构相似,而AsH3的相对分子质量更大,故其分子间作用力比PH3大,所以AsH3的沸点比PH3更高,PH3、AsH3三种物质的沸点由高到低的顺序为NH3﹥AsH3﹥PH3,故答案为:NH3﹥AsH3﹥PH3;NH3之间形成了氢键,分子间作用力大,所以沸点高,AsH3和PH3结构相似,而AsH3的相对分子质量更大,故其分子间作用力比PH3大,所以AsH3的沸点比PH3更高;
(5)K3[Fe(CN)6]中存在离子键、极性共价键、配位键,故答案为:离子键、共价键、配位键;
(6)FeO晶体的晶胞与NaCl的相似,在FeO晶体的晶胞中含有Fe原子或O原子的数目均为4,某氧化亚铁晶体的实际组成为Fe0.9O,则1个晶胞的质量=![]() g,因此该晶体的密度=
g,因此该晶体的密度=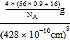 =
=![]() g/cm3,故答案为:
g/cm3,故答案为:![]() 。
。


 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:
【题目】铜及其合金是人类最早使用的金属材料。
(1)基态铜原子的外围电子排布式为_____________。
(2)图1是Cu2O的晶胞,Cu原子配位数为_____________。若Cu2O晶体密度为dgcm-3,晶胞参数为apm,则阿伏加德罗常数值NA=___________。

(3)科学家通过X 射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可表示如图2。
①SO42-中S原子的杂化类型为_______,SO42-的空间构型构型是___________;写出一个与SO42-互为等电子体的分子的化学式__________。
②胆矾的化学式用配合物的形式可表示为___________。1mol 胆矾所含σ键的数目为:_______(设阿伏加德罗常数值NA)
③已知胆矾晶体受热失水分三步。上图2中两个仅以配位键与铜离子结合的水分子最先失去,大致温度为102℃。两个与铜离子以配位键结合,并且与外部的一个水分子以氢键结合的水分子随温度升高而失去,大致温度为113 ℃。而失去最外层水分子所需温度大致为258℃,请分析原因_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家用计算机模拟后确认,60个N原子可结合成N60分子.下列关于N60的叙述中正确的是( )
A.N60是一种新型化合物
B.N60和N2性质完全相同
C.一个N60分子中有30个N2分子
D.N60和N2混合形成的是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法,化合物  的名称是2,3,5,5﹣四甲基﹣4,4﹣二乙基己烷
的名称是2,3,5,5﹣四甲基﹣4,4﹣二乙基己烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色
D.结构片段  的高聚物,其单体是苯酚和甲醛
的高聚物,其单体是苯酚和甲醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )
A.不能通过反应形成高分子化合物
B.不能使酸性KMnO4溶液褪色
C.能发生加成、取代、消去反应
D.1mol该物质最多可与1mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成具有良好生物降解性的有机高分子材料是有机化学研究的重要课题之一.聚醋酸乙烯酯(PVAc)水解生成的聚乙烯醇(PVA),具有良好生物降解性,常用于生产安全玻璃夹层材料PVB.有关合成路线如图(部分反应条件和产物略去).
已知:
Ⅰ.  (R、R′表示烃基或氢)
(R、R′表示烃基或氢)
Ⅱ. 
请回答:
(1)A为饱和一元醇,其氧的质量分数约为34.8%,A的化学名称为 , PVA的结构简式为 .
(2)C中官能团的名称是 , C的名称A~F中核磁共振氢谱出峰最多的是(填化合物代号).
(3)反应①包含的反应类型是;反应④的化学方程式为 .
(4)PVAc是由F加聚而成,与F具有相同官能团的同分异构体还有种;写出其中一种的结构简式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com