
【题目】常温下.Ksp(PbI2)=8.5×10-9。取适量黄色PbI2粉末溶于水中,充分揽拌后得到浊液,过滤。在滤液中加入少量KI,测得c(I-)=1.0×10-2mol·L-1。下列说法正确的是( )
A. Ksp(PbI2)减小 B. 溶液中c(I-)减小
C. 产生黄色沉淀 D. 溶液中c(Pb2+)=8.5×10-7mol·L-1
【答案】C
【解析】常温下.Ksp(PbI2)=8.5×10-9。取适量黄色PbI2粉末溶于水中,充分揽拌后得到浊液,过滤。Ksp(PbI2)= c(Pb2+)![]() c2(I-)=4 c3(Pb2+)=8.5×10-9,所以在滤液中,c(Pb2+)=1.3×10-3 mol·L-1,c(I-)=2.6×10-3mol·L-1。在滤液中加入少量KI,测得c(I-)=1.0×10-2mol·L-1,则c(Pb2+)=
c2(I-)=4 c3(Pb2+)=8.5×10-9,所以在滤液中,c(Pb2+)=1.3×10-3 mol·L-1,c(I-)=2.6×10-3mol·L-1。在滤液中加入少量KI,测得c(I-)=1.0×10-2mol·L-1,则c(Pb2+)=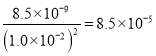 mol·L-1<1.3×10-3 mol·L-1,所以溶液中一定会产生PbI2黄色沉淀。A. Ksp(PbI2)只与温度有关,温度不变,其值不变,A不正确;B. 溶液中c(I-)明显增大了,B不正确;C. 产生黄色沉淀,C正确; D. 溶液中c(Pb2+)=8.5×10-5mol·L-1,D不正确。本题选C。
mol·L-1<1.3×10-3 mol·L-1,所以溶液中一定会产生PbI2黄色沉淀。A. Ksp(PbI2)只与温度有关,温度不变,其值不变,A不正确;B. 溶液中c(I-)明显增大了,B不正确;C. 产生黄色沉淀,C正确; D. 溶液中c(Pb2+)=8.5×10-5mol·L-1,D不正确。本题选C。


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】我国化学家合成了一种新型除草剂的合成路线如下:
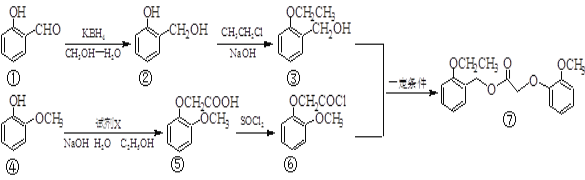
(1)① 中两种含氧官能团的名称_______、_____。除草剂⑦的分子式为_______ 。
(2)③与⑥生成⑦的反应类型是____,④⑤转化中另外一种产物是HCl,则试剂X是_____ 。
(3)写出一种同时满足下列条件的物质③的同分异构体的结构简式______________。
① 属于芳香族化合物; ② 苯环上的一取代物只有两种;
③ 在铜催化下与O2反应,其生成物1 mol与足量的银氨溶液反应生成4 mol Ag
(4)写出②③的化学方程式__________________________________________。
(5)卡巴拉丁是老年人认知障碍的重要治疗药物。请结合上述合成路线及下面所给的反应:![]()
ROH+SOCl2RCl+HOSOCl
请写出合成卡巴拉丁流程中A、B、D的结构简式,C试剂的化学式。
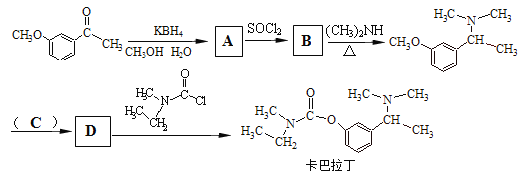
A:____________、B:_____________、C:____________、D:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应过程中,同时有离子键和共价键的断裂和形成的是
A. 2H2+O2![]() 2H2O B. NH3+HCl=NH4Cl
2H2O B. NH3+HCl=NH4Cl
C. 2Na2O2+2H2O=4NaOH+O2↑ D. 2Mg+CO2![]() 2MgO+C
2MgO+C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的有机物,其产量可以作为衡量一个国家石油化工发展水平的标志,F是高分子化合物,有机物A可以实现如下转换关系。请回答下列问题:
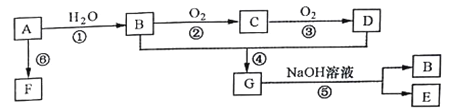
(1)A的结构式为________。
(2)D中含氧原子团的名称为_____,④的化学反应类型为_______。
(3)请分别写出⑤、⑥的化学方程式__________、_________。
(4)在实验室中,可用下图所示装置制取少量G,试管a中盛放的试剂是____,其作用为_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请按要求回答问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中元素______的非金属性最强,元素_____的金属性最强(填元素符号)。
(2)表中元素③的原子结构示意图______;元素⑨形成的氢化物的电子式___________。
(3)表中元素④、⑨形成的氢化物的稳定性顺序为_____> (填化学式)。
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为_____> (填化学式)。
(5)表中元素③、④、⑥、⑦的原子半径大小为____> > > (填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲及其化合物是半导体材料。
(1)25℃时,H2TeO3(亚碲酸):Ka1=1.0×10-3、Ka2=2.0×10-8。在该温度下,0.1mol·L-1H2TeO3溶液的pH约为_____________(填代号)。
A.0.7 B.1 C.2 D.5
NaHTeO3溶液中,H2TeO3、HTeO3-、TeO32-浓度大小的排序为____________________。
(2)工业上,常用铜阳极泥(主要成分是Cu2Te,含少量的Ag、Au)冶炼碲,其工艺流程如下(已知TeO2微溶于水,易与浓强碱.浓强酸反应):
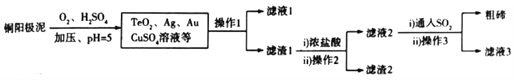
①铜阳极泥溶于硫酸时加压的目的是_____________________________________________;
若调节pH时,pH过低,则粗碲产率会_____________(填“增大”“减小”或“不变”)。
②上述流程中可以循环利用的物质是____________________。
③写出铜阳极泥转化成TeO2的化学方程式:___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积为2L的密闭容器中,加入0.8molA2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+ B2(g) ![]() 2AB(g)ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )
2AB(g)ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )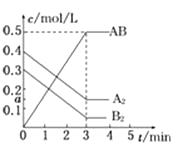
A.图中a点的值为0.15
B.该反应的平衡常数K=0.03
C.温度升高,平衡常数K值减小
D.平衡时A2的转化率为62.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰干电池是最早的实用电池。现用下列工艺回收正极材料中的金属(部分条件未给出)。
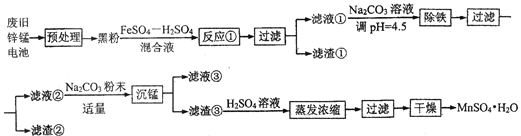
(1)碱性锌锰电池反应为:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH),电解质是KOH,该电池的负极材料为__________(填化学式),MnO(OH)中Mn的化合价为:________,正极反应式为:__________。
(2)黑粉的主要成份为 MnO2和石墨,写出反应①的化学方程式:______。
(3)MnO2的转化率与温度的关系如下表:
温度/℃ | 20 | 40 | 60 | 80 | 100 |
转化率/℃ | 86.0 | 90.0 | 91.3 | 92.0 | 92.1 |
生产中常选反应温度为80℃,其理由是:_______。
(4)“沉锰”过程中生成碱式碳酸锰[MnCO36Mn(OH)25H2O],写出其离子反应方程式:_______,检验沉淀是否洗净的操作是:_______。滤液③中可回收的物质为:________(填化学式)。
(5)“预处理”时,废旧锌锰电池经过拆解、筛分得到炭包,其中含 MnO2为34.8%。称取5.000 g炭包,经处理得到3.211 g MnSO4H2O,计算锰的回收率为:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究 , 其结构简式如图。下列关于分枝酸的叙述正确的是( )

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1 mol分枝酸最多可与3 mol NaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com