
【题目】有机物A是最常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化
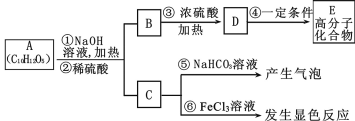
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为:
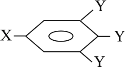 (其中:—X、—Y均为官能团)
(其中:—X、—Y均为官能团)
请回答下列问题:
(1)官能团-X的名称为____,反应③的类型为____;
(2)根据系统命名法,B的名称为____,高聚物E的链节为____;
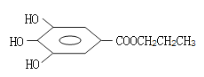
(3)A的结构简式为____;
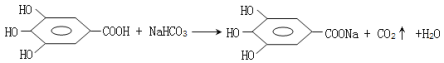
(4)反应⑤的化学方程式为____;
(5)C有多种同分异构体,其中符合下列要求的同分异构体共____种;
i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
(6)从分子结构上看,A具有抗氧化作用的主要原因是____(填序号)。
a 含有苯环 b 含有羰基 c 含有酚羟基
【答案】羧基 消去反应 1-丙醇 ![]()
 3 c
3 c
【解析】
A(C10H12O5)在NaOH水溶液条件下发生水解反应并酸化得到B与C,则A中含有酯基,其中B的相对分子质量为60,分子中只含一个甲基,能在浓硫酸的作用下发生消去反应,则B为CH3CH2CH2OH,B发生消去反应得到D,D为CH3CH═CH2,D发生加聚反应得到高分子化合物E,E为![]() ;C中O原子个数为5,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为
;C中O原子个数为5,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为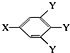 (其中:-X、-Y均为官能团),根据C中氧原子个数知,C为
(其中:-X、-Y均为官能团),根据C中氧原子个数知,C为![]() ,可推知A为
,可推知A为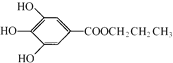 ,据此分析解答。
,据此分析解答。
(1)根据上述分析,C为![]() ,则官能团-X为羧基,反应③为CH3CH2CH2OH发生消去反应生成CH3CH═CH2,故答案为:羧基;消去反应;
,则官能团-X为羧基,反应③为CH3CH2CH2OH发生消去反应生成CH3CH═CH2,故答案为:羧基;消去反应;
(2)根据上述分析,B为CH3CH2CH2OH,根据醇的系统命名法,B的名称为1-丙醇,CH3CH═CH2发生加聚反应得到高分子化合物E为![]() ,高聚物E的链节为
,高聚物E的链节为![]() ,故答案为:1-丙醇;
,故答案为:1-丙醇;![]() ;
;
(3)根据上述分析,A的结构简式为 ,故答案为:
,故答案为: ;
;
(4)反应⑤的化学方程式为![]() +NaHCO3→
+NaHCO3→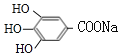 +CO2↑+H2O,故答案为:
+CO2↑+H2O,故答案为:![]() +NaHCO3→
+NaHCO3→ +CO2↑+H2O;
+CO2↑+H2O;
(5)C为![]() ,C的同分异构体符合下列条件:i.含有苯环;ii.能发生银镜反应,说明含有醛基;iii.不能发生水解反应,说明不含酯基,则符合要求的结构简式下:
,C的同分异构体符合下列条件:i.含有苯环;ii.能发生银镜反应,说明含有醛基;iii.不能发生水解反应,说明不含酯基,则符合要求的结构简式下: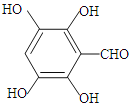 、
、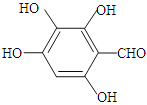 、
、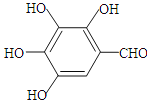 ,共3种,故答案为:3;
,共3种,故答案为:3;
(6)由于苯酚在空气中易被氧化,A分子中有酚羟基,因此A具有抗氧化作用,故答案为:c。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的,如下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化。则下列说法正确的是

A. 通常情况下,NO比N2稳定
B. 通常情况下,N2(g)和O2(g)混合能直接生成NO
C. 1molN2(g)和1molO2(g)具有的总能量小于2mol NO(g)具有的总能量
D. 1molN2(g)和1molO2(g)反应放出的能量为180kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g) ![]() 2HI(g) △H=-a kJ/mol.已知:
2HI(g) △H=-a kJ/mol.已知:
![]() (a、b、c均大于零)。
(a、b、c均大于零)。
下列说法正确的是
A.H2、I2和HI分子中的化学键都是非极性共价键
B.断开2 mol HI分子中的化学键所需能量约为(c+b+a) kJ
C.相同条件下,1 mol H2 (g)和1mol I2 (g)总能量小于2 mol HI (g)的总能量
D.向密闭容器中加入2 mol H2 (g)和2 mol I2 (g),充分反应后放出的热量为2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下左图所示,其中甲池的总反应式为2CH3OH+302+4KOH=2K2CO3+6H20,完成下列问题:

(1)甲池燃料电池的负极反应为___________________。
(2)写出乙池中电解总反应的化学方程式: ___________________。
(3)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生____g沉淀,此时乙池中溶液的体积为400mL,该溶液的pH=____________。
(4)某同学利用甲醇燃料电池设计电解法制取漂白液或Fe(OH)2 的实验装置(如上右图)。若用于制漂白液,a 为电池的______极,电解质溶液最好用_____。若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用___作电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 水的离子积常数KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度
B. Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关
C. 常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,c(NH4+)/c(NH3·H2O)的值增大
D. 室温下,CH3COOH的Ka=1.7×10-5,NH3·H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3·H2O中的c(OH-)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图回答,下列说法不正确的是
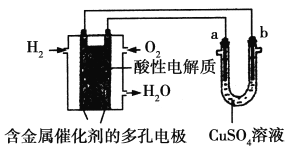
A. 此装置用于铁表面镀铜时,a为铁
B. 此装置用于电镀铜时,硫酸铜溶液的浓度不变
C. 燃料电池中正极反应为1/2O2+2e-+2H+===H2O
D. 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铝是某种高效净水剂的主要成分,实验室利用铝土矿(主要含Al2O3,还含少量Fe2O3、SiO2等杂质)制取碱式氯化铝的过程如下:
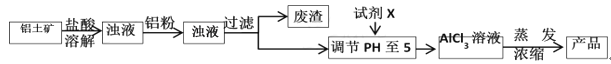
(1)溶解铝土矿需要使用质量分数为15%的盐酸,配制该盐酸所需的玻璃仪器有________
(2)盐酸溶解铝土矿的过程中,发生反应的离子方程式为____________(写一个即可),其目的是__________________________________________________________。
(3)从不引入杂质去考虑,调节溶液的pH时加入的物质最好为__________(填序号)。
A.NaOH B.Al C.氨水 D.Al2O3
(4)写出用pH试纸测定加入试剂X后所得溶液pH的操作:在白瓷板或玻璃片上放一小片pH试纸,________________________________________________,得出被测液的pH。
(5)实验室利用盐酸与大理石制取CO2的实验装置如图所示:
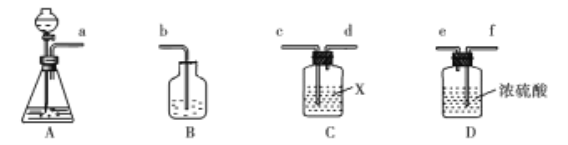
则各装置中导管从左到右的连接顺序为_________,装置C中盛放的试剂X为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是
A. NaHS水解反应:HS-+H2O ![]() H3O++S2-
H3O++S2-
B. Fe(OH)2与稀硝酸反应:2H++Fe(OH)2=Fe2++2H2O
C. 过量的SO2通入到漂白粉溶液中:ClO-+SO2+H2O=HClO+HSO3-
D. Na2CO3水溶液中存在平衡:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式如图所示。下列有关柠檬烯的说法不正确的是( )
![]()
A. 它的核磁共振氢谱有8组吸收峰
B. 它的分子中所有的碳原子不可能在同一平面上
C. 它和丁基苯(![]() )互为同分异构体
)互为同分异构体
D. 一定条件下,它可以发生加成、取代、氧化等反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com