
【题目】下列离子方程式与所述事实相符且正确的是
A. NaHS水解反应:HS-+H2O ![]() H3O++S2-
H3O++S2-
B. Fe(OH)2与稀硝酸反应:2H++Fe(OH)2=Fe2++2H2O
C. 过量的SO2通入到漂白粉溶液中:ClO-+SO2+H2O=HClO+HSO3-
D. Na2CO3水溶液中存在平衡:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
科目:高中化学 来源: 题型:
【题目】家用氯漂白剂的有效成分是NaClO,除用于漂白衣物、消除污渍外,在食品加工中也广泛应用。
Ⅰ.(1)常温下,一定浓度次氯酸钠水溶液的pH=a,则a______7(填>、<或=);结合离子方程式解释其原因是__________________________________________________,此时,溶液中由水电离出的c(OH-)=________mol/L。
(2)漂白剂与酸混合后效果更佳,将0.1000mol/L NaClO溶液与0.1000mol/L 硫酸溶液等体积混合后,关于所得溶液的以下分析正确的是____________(忽略HClO的分解;HSO4-的电离视为完全)。
A.c(HClO)+c(ClO-)=0.1000mol/L
B.c(H+)>c(Na+)=c(SO42-)>c(HClO)>c(ClO-)>c(OH-)
C.c(Na+)+c(H+)=c(SO42-)+c(ClO-)+c(OH-)
D.c(H+)-c(OH-)=2c(ClO-)+c(HClO)
Ⅱ.取20.00g家用氯漂白剂溶液配制成100mL溶液,取出10mL,加入过量KI处理,用足量稀硫酸酸化,然后立即用0.1000mol/L Na2S2O3溶液滴定生成的I2(2Na2S2O3+I2=2I-+Na2S4O6),指示剂显示滴定终点时,消耗Na2S2O3溶液30.00 mL;
(1)用KI处理漂白剂生成I2的离子方程式为________________________________。
(2)该滴定过程选用的指示剂通常为___________,判断滴定终点时的现象是___________________________________________________________________________。
(3)该漂白剂中“有效氯”的含量为_________________(结果保留一位小数)。若滴定结束时,发现滴定管尖嘴部分有气泡,则测定结果________(填“偏高”“偏低”“无影响”)。
注:“有效氯”指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是最常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化
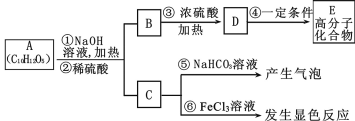
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为:
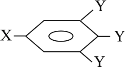 (其中:—X、—Y均为官能团)
(其中:—X、—Y均为官能团)
请回答下列问题:
(1)官能团-X的名称为____,反应③的类型为____;
(2)根据系统命名法,B的名称为____,高聚物E的链节为____;
(3)A的结构简式为____;
(4)反应⑤的化学方程式为____;
(5)C有多种同分异构体,其中符合下列要求的同分异构体共____种;
i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
(6)从分子结构上看,A具有抗氧化作用的主要原因是____(填序号)。
a 含有苯环 b 含有羰基 c 含有酚羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图,下列叙述错误的是( )
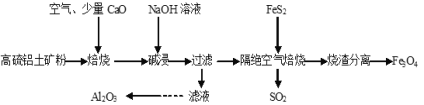
A.烧渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来
B.隔绝空气焙烧时理论上反应消耗的n(FeS2)∶n(Fe2O3)=1∶5
C.向滤液中通入过量CO2、过滤、洗涤、灼烧沉淀可制得Al2O3
D.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是:
A. 铅蓄电池放电时,负极反应式为PbO2+4H++SO![]() +2e-===PbSO4+2H2O
+2e-===PbSO4+2H2O
B. 粗铜精炼时,与电源负极相连的是纯铜,阴极反应式为Cu2++2e-=== Cu
C. 生铁中含碳,抗腐蚀能力比纯铁强
D. 铁制品上镀锌,锌做阴极,铁制品做阳极,电解质溶液中含Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲池是以甲醇为原料,KOH为电解质的高效燃料电池,电化学过程的如图,下列说法中不正确的是

A. 甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O
B. 若乙池中为足量AgNO3溶液,则阳极的电极反应为: 4OH--4e-= 2H2O+O2↑
C. 甲池中随着反应的不断进行,溶液的pH减小
D. 若乙池中为一定量CuSO4溶液,通电一段时间后,向溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯(![]() )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(![]() )、苯甲酸(
)、苯甲酸(![]() )等产品。下表列出了有关物质的部分物理性质,请回答:
)等产品。下表列出了有关物质的部分物理性质,请回答:

注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入2mL甲苯和一定量其它试剂,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。

(1)装置a的名称是_____,主要作用是________。三颈瓶中发生反应的化学方程式为_______。
(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是_________。
(3)反应完毕,反应混合液经过自然冷却至室温后,还应经过__________、________(填操作名称)等操作,才能得到苯甲醛粗产品。
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的实验步骤是______(按步骤顺序填字母)。
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2 d.与适量碳酸氢钠溶液混合振荡
②若对实验①中获得的苯甲酸(相对分子质量为122)产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000 mol/L KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL。产品中苯甲酸的质量分数为_______(保留一位小数)。下列情况会使测定结果偏低的是____(填字母)。
a.滴定终了俯视读取数据 b.KOH标准液长时间接触空气
c.配制KOH标准液时仰视定容 d.将指示剂换为甲基橙溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积。该小组设计的简易实验装置如图所示:
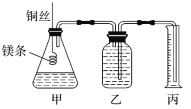
该实验的主要操作步骤如下:
①用已知浓度的浓盐酸配制100mL 1.0mol·L-1的盐酸(需要用到的仪器有量筒、烧杯、__________;
②用10mL的量筒量取8.0mL 1.0mol·L-1的盐酸加入锥形瓶中;
③准确称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为_____;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请回答下列问题:
(1)步骤①中,配制100mL 1.0mol·L-1的盐酸时,下列会使所配制溶液的浓度偏小的操作有____(填字母)。
A 用量筒量取浓盐酸时,俯视量筒的刻度线
B 容量瓶未干燥即用来配制溶液
C 浓盐酸在烧杯中稀释时,搅拌时间过长
D 定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线未做处理
E 在容量瓶中定容时俯视容量瓶刻度线
F 烧杯中有少量水
G 未冷却至室温即定容
(2)实验步骤⑤中应选用的量筒规格是_______
(3)读数时需要注意(至少写两点):______。
(4)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=___L·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填写甲烷与氯气光照时的取代反应现象
(1)试管内气体________________________
(2)试管壁出现_________________________
(3)试管中有少量_________________________
(4)水面___________,但____________(填“充满”“ 不充满”)整个试管。
(5)产物中共有_______ 种,其中____________的结构是正四面体(写名称)写出第一步取代反应:______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com