
【题目】下列离子方程式书写正确的是( )
A.食醋除水垢:![]()
B.稀硝酸中加入少量亚硫酸钠:![]()
C.处理工业废水时Cr(Ⅵ)的转化:![]()
D.用酸性KMnO4测定草酸溶液浓度:![]()
科目:高中化学 来源: 题型:
【题目】研究生铁的锈蚀,下列分析不正确的是
序号 | ① | ② | ③ |
实验 |
|
|
|
现象 | 8小时未观察 到明显锈蚀 | 8小时未观察 到明显锈蚀 | 1小时观察 到明显锈蚀 |
A. ①中,NaCl溶液中溶解的O2不足以使生铁片明显锈蚀
B. ②中,生铁片未明显锈蚀的原因之一是缺少H2O
C. ③中正极反应:O2+4e+ 2H2O ==4OH
D. 对比①②③,说明苯能隔绝O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2。E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
(1)物质X的名称__________________。![]()
![]()
![]()
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因_____________________
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:________________________________________________________。
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有__________________。
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为___________________________________________________。将所得沉淀过滤、洗涤、灼烧,可得到___________g固体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到直观形象的效果,下列表达不正确的是( )
A. NaOH溶液与SO2反应时溶液中溶质的情况 ![]()
B. NaAlO2溶液与盐酸反应后铝的存在形式![]()
C. Fe在Cl2中燃烧产物![]()
D. Fe和稀硝酸反应后,铁的存在形式![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将由FeSO4、Ba(OH)2、AlCl3三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是( )
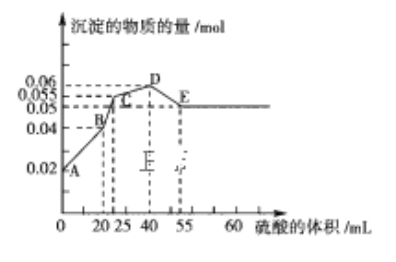
A. AB段发生反应的离子方程式为:Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O
B. D点表示的溶液呈酸性
C. C点表示的沉淀的化学式为Al(OH)3、BaSO4、Fe(OH)2
D. 混合物中FeSO4和AlCl3的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+O2(g)===CO2(g) ΔH1
CO2(g)+C(s)===2CO(g) ΔH2
2CO(g)+O2(g)===2CO2(g) ΔH3
4Fe(s)+3O2(g)===2Fe2O3(s) ΔH4
3CO(g)+Fe2O3(s)===3CO2(g)+2Fe(s) ΔH5
下列关于上述反应焓变的判断正确的是
A. ΔH1>0,ΔH3<0B. ΔH2>0,ΔH4>0C. ΔH1=ΔH2+ΔH3D. ΔH3=ΔH4+ΔH5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示。A元素的某种同位素原子没有中子,D元素的原子序数是C的2倍,E是短周期主族元素中半径最大的元素。下列说法不正确的是
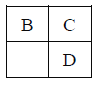
A. 简单离子的半径大小关系:B>C>E
B. D、E两种元素形成的化合物,可能含有离子键和共价键
C. A、B、C三种元素形成的化合物的水溶液均显酸性
D. D、E分别和C形成的化合物,均可能使溴水或品红溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X含有K+、Mg2+、Fe3+、Al3+、Fe2+、Cl-、CO32-、OH-、SiO32-、NO3-、SO42-中的几种,已知该溶液中各离子物质的量浓度均为0.20mol·L-1(不考虑水的电离及离子的水解)。为确定该溶液中含有的离子,现进行了如下的操作:
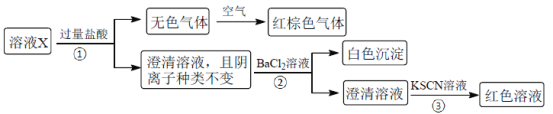
下列说法正确的是
A.无色气体可能是NO和CO2的混合物
B.由步骤③可知,原溶液肯定存在Fe3+
C.溶液X中所含离子种类共有4种
D.另取100mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为2.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把8.0g铁粉投入40mL某HNO3溶液中,充分反应后剩余固体2.4g,产生NO2和NO的混合气体0.12mol。若不考虑N2O4的存在,则原HNO3溶液的物质的量浓度( )
A.6.0mol·L-1B.7.0mol·L -1C.8.0mol·L -1D.9.0mol·L -1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com