
【题目】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2。E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
(1)物质X的名称__________________。![]()
![]()
![]()
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因_____________________
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:________________________________________________________。
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有__________________。
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为___________________________________________________。将所得沉淀过滤、洗涤、灼烧,可得到___________g固体。
【答案】过氧化钠 Al与氧气反应生成的氧化铝熔点高,在Al表面好像一层膜兜着,因此熔化的铝不滴落  BC 2Na + 2H2O+ Cu2+ === Cu(OH)2 ↓ + 2Na+ + H2 ↑
BC 2Na + 2H2O+ Cu2+ === Cu(OH)2 ↓ + 2Na+ + H2 ↑ ![]()
【解析】
A的一种单质是自然界硬度最大的物质,是金刚石,则A为碳;B与C的单质在加热条件下反应生成淡黄色化合物X,为过氧化钠,则B为氧,C为钠;D的单质既能与盐酸、也能与NaOH溶液反应生成H2,说明D为铝,E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y,说明E为铁,生成四氧化三铁。
(1)根据分析得到物质X的名称为过氧化钠,故答案为过氧化钠。
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因Al与氧气反应生成的氧化铝熔点高,在Al表面好像一层膜兜着,因此熔化的铝不滴落,故答案为:Al与氧气反应生成的氧化铝熔点高,在Al表面好像一层膜兜着,因此熔化的铝不滴落。
(3) E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:
 ,故答案为:
,故答案为:![]() 。
。
(4)ag 钠投入足量CuSO4溶液中,“浮”、“熔”、“游”、“嘶”“蓝”,因此实验现象正确的是B.熔化成银色光亮的小球,C.小球四处游动发出”嘶嘶”的声音,可能的离子方程式为2Na + 2H2O+ Cu2+ =Cu(OH)2 ↓ + 2Na+ + H2 ↑,
根据守恒2Na ——Cu(OH)2 ↓——CuO
46g 80g
ag xg
46g:ag = 80g:xg
解得x =![]() ,故答案为:BC;2Na + 2H2O+Cu2+=Cu(OH)2 ↓+2Na++H2 ↑;
,故答案为:BC;2Na + 2H2O+Cu2+=Cu(OH)2 ↓+2Na++H2 ↑;![]() 。
。


科目:高中化学 来源: 题型:
【题目】核电荷数依次增大的A、B、C、D、E、F都是周期表中前四周期的元素,其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,AC2为非极性分子,B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,E原子的一种核素的质量数为49,中子数为27。F元素是第四周期元素中未成对电子数最多的元素,FCl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,1mol配合物与足量的AgNO3溶液反应能立即生成3molAgCl。请根据以上情况,回答下列问题:(答题时需用元素符号表示)
(1)B氢化物与HCl反应生成的含有B元素粒子的空间构型是___________;F元素原子的最外层电子数为________个。
(2)B3-离子分别与AC2及由B、C组成的气态化合物互为等电子体,则B、C组成的化合物化学式为_______________;B3-离子还可以和某一价阴离子互为等电子体,该阴离子电子式为_________,这种阴离子常用于检验日常生活中的一种金属阳离子,则金属阳离子符号为_________。
(3)B元素与同周期相邻元素的第一电离能由小到大的顺序为_______________。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应中氧化剂与还原剂的物质的量之比是_______________。
(5)F3+的核外电子排布式是_________________________,FCl3形成的六配位的配合物化学式为________________________。
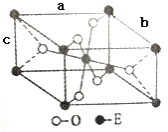
(6)E的一种氧化物晶胞结构(长方体)如图所示,该氧化物的化学式为__________;若该晶胞的三个晶胞参数分别为:apm、bpm、cpm。则该氧化物的密度为____________g/cm3。(写出表达式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
(装置分析)
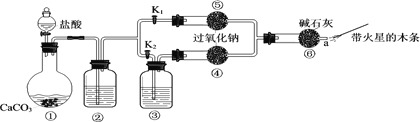
(1)装置①中反应的离子方程式是______。
(2)装置②中的试剂是______(填序号)。
a.饱和Na2CO3溶液 b.饱和NaHCO3溶液 c.浓H2SO4
(3)装置③中的试剂是______。
(进行实验)步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。 步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(4)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是______。
(5)过氧化钠跟二氧化碳反应的化学方程式是______。
(实验反思)
(6)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应。”其理由是______。
(7)需要补充的实验操作是:取⑤中反应后的少量固体,______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时:①HF(aq)+OH-(aq)![]() F-(aq)+H2O(l) ΔH=-67.7 kJ/mol
F-(aq)+H2O(l) ΔH=-67.7 kJ/mol
②H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol下列有关说法中正确的是( )
A.HF电离:HF(aq)![]() H+(aq)+F-(aq)△H=+10.4KJ/mol
H+(aq)+F-(aq)△H=+10.4KJ/mol
B.水解消耗0.1 mol F-时,吸收的热量为6.77 kJ
C.中和热均为57.3 kJ/mol
D.含1 mol HF、1 mol NaOH的两种溶液混合后放出的热量为67.7 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①将0.100 L 1.00 mol·L-1的纯碱溶液逐滴滴入0.100 L 1.25 mol·L-1的盐酸中;②将0.100 L 1.25 mol·L-1的盐酸逐滴滴入0.100 L 1.00 mol·L-1的纯碱溶液中;两种操作产生CO2的体积比为
A. 5∶2 B. 2∶5 C. 2∶1 D. 1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定的溶液中能大量共存的是( )
A.常温下,水电离的c(OH-)= 1×10-12mo1·L-1的溶液中:![]()
B.能使酚酞变红的溶液中:![]()
C.0. 1 mol·L1KI 溶液:![]()
D.常温下,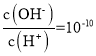 的溶液中:
的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述不正确的是( )
A.体积②>③>①>④B.密度②>③>④>①
C.质量②>③>④>①D.氢原子个数①>③>④>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.食醋除水垢:![]()
B.稀硝酸中加入少量亚硫酸钠:![]()
C.处理工业废水时Cr(Ⅵ)的转化:![]()
D.用酸性KMnO4测定草酸溶液浓度:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,在25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L醋酸溶液,曲线如图所示。有关粒子浓度大小关系的比较正确的是( )
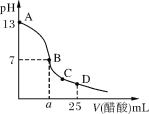
A.在A、B间任一点(不包含A、B两点),溶液中一定有:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.在B点,a>12.5,且有:c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com