
【题目】核电荷数依次增大的A、B、C、D、E、F都是周期表中前四周期的元素,其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,AC2为非极性分子,B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,E原子的一种核素的质量数为49,中子数为27。F元素是第四周期元素中未成对电子数最多的元素,FCl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,1mol配合物与足量的AgNO3溶液反应能立即生成3molAgCl。请根据以上情况,回答下列问题:(答题时需用元素符号表示)
(1)B氢化物与HCl反应生成的含有B元素粒子的空间构型是___________;F元素原子的最外层电子数为________个。
(2)B3-离子分别与AC2及由B、C组成的气态化合物互为等电子体,则B、C组成的化合物化学式为_______________;B3-离子还可以和某一价阴离子互为等电子体,该阴离子电子式为_________,这种阴离子常用于检验日常生活中的一种金属阳离子,则金属阳离子符号为_________。
(3)B元素与同周期相邻元素的第一电离能由小到大的顺序为_______________。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应中氧化剂与还原剂的物质的量之比是_______________。
(5)F3+的核外电子排布式是_________________________,FCl3形成的六配位的配合物化学式为________________________。
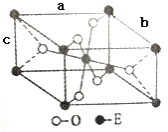
(6)E的一种氧化物晶胞结构(长方体)如图所示,该氧化物的化学式为__________;若该晶胞的三个晶胞参数分别为:apm、bpm、cpm。则该氧化物的密度为____________g/cm3。(写出表达式即可)
【答案】正四面体形 1 N2O ![]() Fe3+ C<O<N 1:4 1s22s22p63s23p63d3或[Ar]3d3 [Cr(NH3)4(H2O)2]Cl3 TiO2
Fe3+ C<O<N 1:4 1s22s22p63s23p63d3或[Ar]3d3 [Cr(NH3)4(H2O)2]Cl3 TiO2 ![]()
【解析】
A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,C形成-2价阴离子,且D位于C的下一周期,B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,分子中存在氢键,C形成-2价阴离子,则C为氧元素,故D为镁元素;核电荷数B<C,则B为氮元素;A、B、C是同一周期的非金属元素,AC2为非极性分子,则A为碳元素;E原子的一种核素的质量数为49,中子数为27,则质子数为22,E为Ti元素。F元素是第四周期元素中未成对电子数最多的元素,原子核外电子排布为:1s22s22p63s23p63d54s1,则F为Cr元素;CrCl3能与NH3、H2O形成六配位的配合物,且两种配体的物质的量之比为2:1,则配体中有4个NH3、2个H2O,1mol配合物与足量的AgNO3溶液反应能立即生成3molAgCl,说明三个氯离子位于外界,该配合物为[Cr(NH3)4(H2O)2]Cl3,据此分析解题。
由分析知:A为C元素、B为N元素、C为O元素、D为Mg元素、E为Ti元素、F为Cr元素;
(1)N元素氢化物与HCl反应生成的含有N元素粒子为NH4+,分子中N原子价层电子对数=4+![]() =4、N原子为sp3杂化,不含孤对电子,故其空间构型是正四面体;F为Cr,原子核外电子排布为1s22s22p63s23p63d54s1,元素原子的最外层电子数为1个;
=4、N原子为sp3杂化,不含孤对电子,故其空间构型是正四面体;F为Cr,原子核外电子排布为1s22s22p63s23p63d54s1,元素原子的最外层电子数为1个;
(2)N3-离子分别与CO2、由N、O组成的气态化合物互为等电子体,则N、O组成的化合物化学式为N2O;N3-离子还可以和一价阴离子互为等电子体,根据价电子总数相等,用S、C原子代替2个N原子可知该阴离子为SCN-,结构与CO2类似,这阴离子电子式为![]() ,这种阴离子常用于检验日常生活中的一种金属阳离子,这金属阳离子符号为Fe3+;
,这种阴离子常用于检验日常生活中的一种金属阳离子,这金属阳离子符号为Fe3+;
(3)同周期自左而右第一电离能呈增大趋势,氮元素原子2p能级有3个电子,处于半满稳定状态,电子能量低,氮元素第一电离能高于相邻的元素的,所以第一电离能由小到大的顺序为C<O<N;
(4)B的最高价氧化物对应的水化物为HNO3,D的单质为Mg,HNO3稀溶液与Mg反应时,N元素被还原到最低价,则生成NH4NO3,Mg被氧化为Mg(NO3)2,令NH4NO3,Mg(NO3)2的化学计量数分别为x、y,则根据电子转移守恒有[5-(-3)]×x=2y,所以x:y=4:1,该反应的化学方程式是4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O,所以该反应中氧化剂与还原剂的物质的量之比是1:4;
(5)Cr原子核外电子排布为:1s2222p63s23p63d54s1,Cr原子失去4s能级1个电子、3d能级2个电子形成Cr3+,Cr3+的核外电子排布式是1s22s22p63s23p63d3,由上述分析可知,CrCl3形成的六配位的配合物化学式为[Cr(NH3)4(H2O)2]Cl3;
(6)由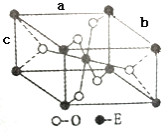 可知,晶胞中Ti原子位于体心与顶点上,O原子位于上下两个面上及体内(有2个),故晶胞中Ti元素数目=1+8×
可知,晶胞中Ti原子位于体心与顶点上,O原子位于上下两个面上及体内(有2个),故晶胞中Ti元素数目=1+8×![]() =2、O原子数目=2+4×
=2、O原子数目=2+4×![]() =4,故该化合物化学式为TiO2,晶胞质量=2×
=4,故该化合物化学式为TiO2,晶胞质量=2×![]() g,若晶胞中参数分别为apm、bpm、cpm,则晶胞的体积=a×10-10cm×b×10-10cm×c×10-10cm=abc×10-30cm3,该晶体的密度=
g,若晶胞中参数分别为apm、bpm、cpm,则晶胞的体积=a×10-10cm×b×10-10cm×c×10-10cm=abc×10-30cm3,该晶体的密度=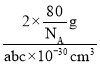 =
=![]() g/cm3。
g/cm3。


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
【题目】化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )
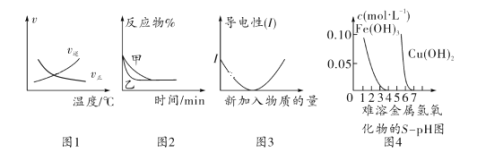
A.根据图1可判断可逆反应“A2(g)+3B2(g)![]() 2AB3(g)”的 ΔH<0
2AB3(g)”的 ΔH<0
B.图2可能表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
C.图3可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.根据图4,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,请回答有关问题:

(1)①的元素符号为 _________;
(2)第3周期主族元素中,原子半径最小的是_________(用元素符号表示)。
(3)表中元素的气态氢化物中最稳定的是______________(用化学式表示)。
(4)①、②、⑦、⑧四种元素的最高价氧化物的水化物中酸性最强的是______(用化学式表示)。
(5)①和⑧形成化合物的电子式为_________________
(6)④和⑥两种元素的最高价氧化物的水化物在水溶液中反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。液体A和气体B的组合不可能是( )
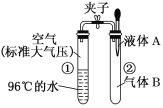
A. 氢氧化钠溶液、一氧化氮
B. 水、氨气
C. 氢氧化钠溶液、二氧化碳
D. 水、二氧化氮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物广泛存在于自然界。请回答下列问题:
(1)反应Ⅰ:Fe(s)+CO2(g) ![]() FeO(s)+CO(g) ΔH1 平衡常数为K1
FeO(s)+CO(g) ΔH1 平衡常数为K1
反应Ⅱ:Fe(s)+H2O(g) ![]() FeO(s)+H2(g) ΔH2 平衡常数为K2
FeO(s)+H2(g) ΔH2 平衡常数为K2
不同温度下,K1、K2的值如下表:
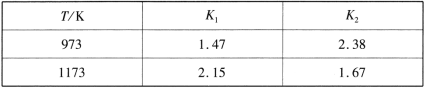
现有反应Ⅲ:H2(g)+CO2(g) ![]() CO(g)+H2O(g),结合上表数据,反应Ⅲ是_______ (填“放热”或“吸热”)反应。
CO(g)+H2O(g),结合上表数据,反应Ⅲ是_______ (填“放热”或“吸热”)反应。
(2)已知CO2催化加氢合成乙醇的反应原理为:
2CO2(g)+6H2(g) ![]() C2H5OH(g)+3H2O(g) H<0。
C2H5OH(g)+3H2O(g) H<0。
设m为起始时的投料比,即m= n(H2)/ n(CO2)。
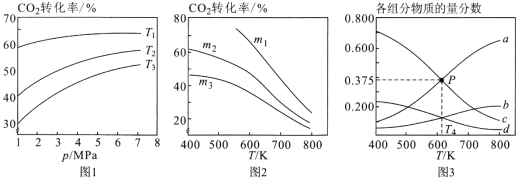
①图1中投料比相同,温度从高到低的顺序为______________________。
②图2中m1、m2、m3从大到小的顺序为________________________。
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质化学名称为______________,T4温度时,该反应平衡常数KP的计算式为(不必化简)_______________________。
(3)已知:NH3·H2O的Kb=1.7×10-5,H2CO3的Ka1=4.3×10-7、Ka2=5.6×10-11。工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5℃~26.5℃后用氨水吸收过量的CO2。所得溶液的pH___________7(填“>”、“=”或“<”)。烟气需冷却至15.5℃~26.5℃的可能原因是____________。
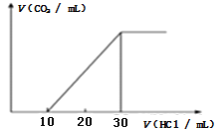
(4)为了测量某湖水中无机碳含量,量取100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收。往吸收液中滴加1.0mol/L盐酸,生成的V(CO2)随V(盐酸)变化关系如图所示,则原吸收液中离子浓度由大到小的顺序为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度和压强相同时,在体积相同的两个密闭容器甲和乙,甲中充满O2气体,乙中充满O2和O3的混合气体,下列说法正确的是
A. 两容器中气体的质量相等 B. 两容器中气体的分子数目相等
C. 两容器中气体的氧原子数目相等 D. 两容器中气体的密度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只能被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是( )
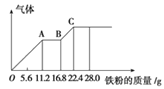
A. 混合酸液中NO3-的物质的量为0.4 mol
B. OA段产生是NO,AB段反应为2Fe3++Fe=3Fe2+,BC段产生氢气
C. 溶液中最终溶质为FeSO4
D. c(H2SO4)为5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究生铁的锈蚀,下列分析不正确的是
序号 | ① | ② | ③ |
实验 |
|
|
|
现象 | 8小时未观察 到明显锈蚀 | 8小时未观察 到明显锈蚀 | 1小时观察 到明显锈蚀 |
A. ①中,NaCl溶液中溶解的O2不足以使生铁片明显锈蚀
B. ②中,生铁片未明显锈蚀的原因之一是缺少H2O
C. ③中正极反应:O2+4e+ 2H2O ==4OH
D. 对比①②③,说明苯能隔绝O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2。E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
(1)物质X的名称__________________。![]()
![]()
![]()
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因_____________________
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:________________________________________________________。
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有__________________。
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为___________________________________________________。将所得沉淀过滤、洗涤、灼烧,可得到___________g固体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com