
【题目】在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述不正确的是( )
A.体积②>③>①>④B.密度②>③>④>①
C.质量②>③>④>①D.氢原子个数①>③>④>②
【答案】C
【解析】
①6.72LCH4的物质的量n=![]() =6.72L÷22.4L/mol=0.3mol;
=6.72L÷22.4L/mol=0.3mol;
②3.01×1023个HCl的物质的量n=![]() =3.01×1023÷6.02×1023/mol=0.5mol;
=3.01×1023÷6.02×1023/mol=0.5mol;
③13.6gH2S的物质的量n=13.6g÷34g/mol=0.4mol;
④0.2molNH3。
A.根据V=n·Vm知,相同条件下体积之比等于物质的量之比,所以体积②>③>①>④,A正确,不符合题意;
B.根据ρ=![]() 可知,相同条件下,气体的密度之比等于摩尔质量之比,所以气体的密度关系为②>③>④>①,B正确,不符合题意;
可知,相同条件下,气体的密度之比等于摩尔质量之比,所以气体的密度关系为②>③>④>①,B正确,不符合题意;
C.根据m=n·M知,甲烷质量m(CH4)=0.3mol×16g/mol=4.8g,HCl的质量m(HCl)=0.5mol×36.5g/mol=18.25g,氨气的质量m(NH3)=0.2mol×17g/mol=3.4g,故气体的质量关系②>③>①>④,C错误,符合题意;
D.甲烷中n(H)=0.3mol×4=1.2mol,HCl中n(H)=0.5mol×1=0.5mol,硫化氢中n(H)=0.4mol×2=0.8mol,氨气中n(H)=0.2mol×3=0.6mol,故四种气体中的H原子数目①>③>④>②,D正确,不符合题意;
故合理选项是C。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只能被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是( )
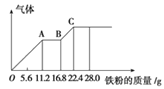
A. 混合酸液中NO3-的物质的量为0.4 mol
B. OA段产生是NO,AB段反应为2Fe3++Fe=3Fe2+,BC段产生氢气
C. 溶液中最终溶质为FeSO4
D. c(H2SO4)为5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物,如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下:
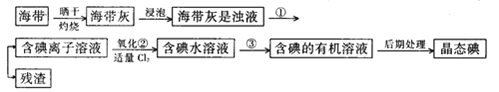
(1)指出提取碘的过程中有关的实验操作名称:①____________________;③______________________。写出实验②中有关反应的离子方程式___________________________________________。
(2)提取碘的过程中,可供选择的有关试剂是___________。
A. 甲苯、酒精 B. 四氯化碳、苯 C. 汽油、乙酸 D. 汽油、甘油
(3)为使海带中I-转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器。还缺少的仪器是________。
(4)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出下图实验装置中的错误之处:①_________________②___________________③___________________。
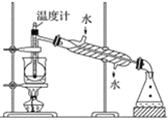
(5)进行上述蒸馏操作时,使用水浴的原因是___________;最后,晶态碘在___________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2。E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
(1)物质X的名称__________________。![]()
![]()
![]()
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因_____________________
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:________________________________________________________。
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有__________________。
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为___________________________________________________。将所得沉淀过滤、洗涤、灼烧,可得到___________g固体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中,不能够按照![]() (“→”表示一步完成)关系相互转化的是( )
(“→”表示一步完成)关系相互转化的是( )
物质 选项 | a | b | c |
A | Na | Na2O2 | NaCl |
B | AlCl3 | Al(OH)3 | NaAlO2 |
C | FeO | Fe(NO3)2 | Fe(OH)2 |
D | CuO | CuSO4 | Cu(OH)2 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到直观形象的效果,下列表达不正确的是( )
A. NaOH溶液与SO2反应时溶液中溶质的情况 ![]()
B. NaAlO2溶液与盐酸反应后铝的存在形式![]()
C. Fe在Cl2中燃烧产物![]()
D. Fe和稀硝酸反应后,铁的存在形式![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将由FeSO4、Ba(OH)2、AlCl3三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是( )
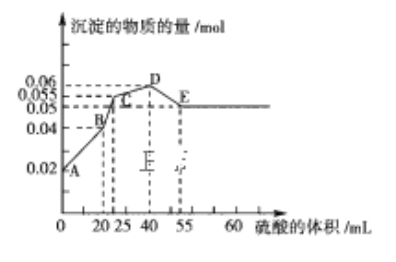
A. AB段发生反应的离子方程式为:Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O
B. D点表示的溶液呈酸性
C. C点表示的沉淀的化学式为Al(OH)3、BaSO4、Fe(OH)2
D. 混合物中FeSO4和AlCl3的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示。A元素的某种同位素原子没有中子,D元素的原子序数是C的2倍,E是短周期主族元素中半径最大的元素。下列说法不正确的是
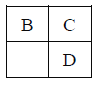
A. 简单离子的半径大小关系:B>C>E
B. D、E两种元素形成的化合物,可能含有离子键和共价键
C. A、B、C三种元素形成的化合物的水溶液均显酸性
D. D、E分别和C形成的化合物,均可能使溴水或品红溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业。其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
(1)K3[Fe(CN)6]中所涉及的元素的基态原子核外未成对电子数最多的是_________(填元素名称),各元素的第一电离能由大到小的顺序为___________________。
(2)(CN)2分子中存在碳碳键,则分子中σ键与π键数目之比为_______。
(3)CO能与金属Fe形成Fe(CO)5,该化合物熔点为253 K,沸点为为376 K,其固体属于_________晶体。
(4)下图是金属单质常见的两种堆积方式的晶胞模型。
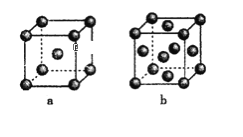
①铁采纳的是a堆积方式.铁原子的配位数为_____,该晶体中原子总体积占晶体体积的比值为_________(用含π的最简代数式表示)。
②常见的金属铝采纳的是b堆积方式,铝原子的半径为r pm,则其晶体密度为__________g·cm-3(用含有r、NA的最简代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com