
【题目】某化学实验小组的同学为探究和比较SO2和氯水漂白性的强弱,设计了如下的实验装置。
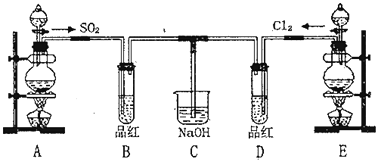
(1)实验室用装置A制备SO2.某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是_____
(2)实验室用装置E制备Cl2,写出反应的化学方程式_____请指出该反应中的液体反应物在反应中所表现出的化学性质_____。若液体反应物中的溶质反应了6mol,则标准状况下生成Cl2的体积为_____L
(3)停止通气后,再给BD两个试管分别加热,两个试管中的现象分别为:B_____、D_____
(4)C装置的作用是吸收尾气,防止污染空气,写出吸收Cl2的离子方程式_____
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通到品红溶液中,结果发现溶液基本不褪色。请你分析该现象的原因_____(用化学方程式表示)
【答案】分液漏斗的玻璃塞没有取下来 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 酸性和还原性 33.6 褪色的品红又恢复成红色 溶液没有明显变化 Cl2+2OH-=Cl-+ClO-+H2O Cl2+SO2+2H2O=2HCl+H2SO4
MnCl2+Cl2↑+2H2O 酸性和还原性 33.6 褪色的品红又恢复成红色 溶液没有明显变化 Cl2+2OH-=Cl-+ClO-+H2O Cl2+SO2+2H2O=2HCl+H2SO4
【解析】
A用于制备SO2,可用Na2SO3与硫酸反应制取,B用于检验二氧化硫的生成,E用浓盐酸和二氧化锰在加热条件下MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O制备氯气,D用于检验气体的漂白性,C用于吸收尾气。
MnCl2+Cl2↑+2H2O制备氯气,D用于检验气体的漂白性,C用于吸收尾气。
(1)塞子没有取下来,打开活塞时,空气无法进入分液漏斗内部,从而造成分液漏斗内的压强小于大气压强。
(2)实验室中用二氧化锰固体与浓盐酸加热反应制备氯气,方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,反应中HCl被氧化生成Cl2,表现出还原性;反应生成盐,表现出酸性。由方程式可知,6molHCl参加反应生成氯气:6mol×
MnCl2+Cl2↑+2H2O,反应中HCl被氧化生成Cl2,表现出还原性;反应生成盐,表现出酸性。由方程式可知,6molHCl参加反应生成氯气:6mol×![]() =1.5mol,则生成的氯气的体积为1.5mol×22.4L/mol。
=1.5mol,则生成的氯气的体积为1.5mol×22.4L/mol。
(3)次氯酸的漂白性是永久性的,加热也不会改变反应产物;二氧化硫的漂白是暂时的,加热时,无色的产物会分解,又生成原来的反应物。
(4)用氢氧化钠溶液吸收氯气,生成氯化钠、次氯酸钠和水。
(5)氯气具有较强的氧化性,二氧化硫具有较强的还原性,在水溶液中两者1:1发生反应生成没有漂白性的产物。
(1)塞子没有取下来,打开活塞时,空气无法进入分液漏斗内部,造成分液漏斗内的压强小于大气压强,液体无法流出。答案为:分液漏斗的玻璃塞没有取下来;
(2)实验室中用二氧化锰固体与浓盐酸加热反应制备氯气,反应的方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,反应中HCl被氧化表现还原性,同时生成盐表现酸性;由方程式可知,6molHCl参加反应生成氯气:6mol×
MnCl2+Cl2↑+2H2O,反应中HCl被氧化表现还原性,同时生成盐表现酸性;由方程式可知,6molHCl参加反应生成氯气:6mol×![]() =1.5mol,则生成的氯气的体积为1.5mol×22.4L/mol=33.6L。答案为:MnO2+4HCl(浓)
=1.5mol,则生成的氯气的体积为1.5mol×22.4L/mol=33.6L。答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;酸性和还原性;33.6;
MnCl2+Cl2↑+2H2O;酸性和还原性;33.6;
(3)次氯酸的漂白性是永久性的,二氧化硫的漂白性是暂时的。加热时,次氯酸漂白过的溶液无变化,二氧化硫和有色物质生成的无色物质不稳定,加热时会变成红色。答案为:褪色的品红又恢复成红色;溶液没有明显变化;
(4)用氢氧化钠溶液吸收氯气,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O。答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(5)氯气具有较强的氧化性,二氧化硫具有较强的还原性,在水溶液中两者1:1发生反应Cl2+SO2+2H2O=2HCl+H2SO4,生成物都无漂白性,因而SO2和Cl2按1:1同时通入到品红溶液时,品红溶液并不褪色。答案为:Cl2+SO2+2H2O=2HCl+H2SO4。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】一定温度下恒容容器中,可逆反应![]() 达到平衡状态的标志是
达到平衡状态的标志是
①单位时间内生成n mol H2的同时生成2n mol HI
②单位时间内生成n mol H2的同时,生成n molI2
③用HI、I2、H2的物质的量浓度变化表示的反应速率的比为2∶1∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的压强不再改变的状态
A.①④ .B.①④⑤ .C.①②④⑤ .D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示物质A~F之间的转化关系,其中A为淡黄色固体物质,B、C为无色溶液,D为气体,E、F为白色沉淀。请填写下列各空:
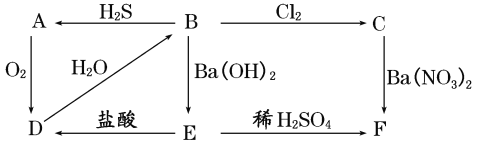
(1)写出各物质的化学式:
A为______,B为_____,C为_____,D为_____,E为_____,F为______。
(2)写出下列反应的化学方程式:
B→A:________________________。
B→C:___________________________。
(3)写出C→F的离子方程式:___________________。
(4)在A~F六种物质中,既有氧化性又有还原性的是(填字母代号)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置是某次实验最初的情况(夹持装置省略),烧瓶内盛有等体积的甲烷和氯气,用光照射烧瓶一段时间,下列说法正确的是( )
![]()
A. 只能生成CH3Cl一种有机物
B. 烧瓶内液面不可能上升
C. 大试管内的液体可能会分层
D. 向水中加入石蕊试液后不变色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下浓度为0.1mol·L-1的下列溶液的pH如下表:
溶质 | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
下列有关说法正确的是
A. 在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B. 若将CO2通入0.1 mol·L-1Na2CO3溶液中至溶液中性,则溶液中2c(CO32-)+c(HCO3-)=0.1 mol·L-1
C. 根据上表,水解方程式ClO-+H2O![]() HClO+OH-的水解常数K=10-7.6
HClO+OH-的水解常数K=10-7.6
D. 向上述NaClO溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>c(H+)>c(HClO)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素.霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾.
(1)SO2在烟尘的催化下形成硫酸的反应方程式是______________.
(2)NOx和SO2在空气中存在下列平衡:
2NO(g)+O2(g)2NO2(g)△H=﹣113.0kJmol﹣1
2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol﹣1
SO2通常在二氧化氮的存在下,进一步被氧化,生成SO3.
①写出NO2和SO2反应的热化学方程式为_________.
②随温度升高,该反应化学平衡常数变化趋势是_____.
(3)提高2SO2+O22SO3反应中SO2的转化率,是减少SO2排放的有效措施.
①T温度时,在1L的密闭容器中加入2.0mol SO2和1.0mol O2,5min后反应达到平衡,二氧化硫的转化率为50%,该反应的平衡常数是____.
②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是_____(填字母).
a.温度和容器体积不变,充入1.0mol He b.温度和容器体积不变,充入1.0mol O2
c.在其他条件不变时,减少容器的体积 d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度
(4)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图。

①电解饱和食盐水的化学方程式是________________.
②用溶液A吸收含二氧化硫的废气,其反应的离子方程式是_________.
③用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的浓HNO3中投入1.28gCu,Cu完全溶解,生成气体颜色越来越浅,共收集到气体448mL(标准状况),将盛有此气体的容器倒扣在水槽中,再通入一定体积的O2,恰好使气体完全溶于水,则通入O2的体积(标准状况)为
A.504mLB.336mLC.224mLD.448mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
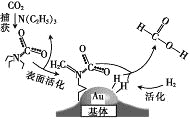
A. 标准状况下,22.4L CO2中所含的电子数目为16NA
B. 10.1g N(C2H5)3中所含的非极性共价键数目为0.3NA
C. 2mol Au与2mol H2中所含的分子数目均为2NA
D. 100g 46%的甲酸水溶液中所含的氧原子数目为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生化学实验小组,为验证非金属元素氟的氧化性强于硫和氮,设计了一套实验装置:(部分加持装置已略去)
(1)写出A中反应的离子方程式 。
(2)B中出现黄色浑浊现象,产生此现象的离子方程式 。
(3)试从原子结构角度解释氯的氧化性大于硫的原因 。
(4)D中干燥管中出现的现象及化学方程式 。
(5)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,请画出其装置图 (并注明盛装试剂)。
(6)还有什么方法能证明氧化性Cl2>S,用一种相关事实说明 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com