
【题目】一定温度下恒容容器中,可逆反应![]() 达到平衡状态的标志是
达到平衡状态的标志是
①单位时间内生成n mol H2的同时生成2n mol HI
②单位时间内生成n mol H2的同时,生成n molI2
③用HI、I2、H2的物质的量浓度变化表示的反应速率的比为2∶1∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的压强不再改变的状态
A.①④ .B.①④⑤ .C.①②④⑤ .D.①②③④⑤
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.在镀件上电镀铜时,镀件应连接电源的负极
B.粗铜电解精炼时,若电路中通过2 mol e-,阳极减少64g
C.用惰性电极电解MgCl2溶液所发生反应的离子方程式为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D.用惰性电极电解饱和食盐水,阴极逸出的气体可使湿润的淀粉碘化钾试纸变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
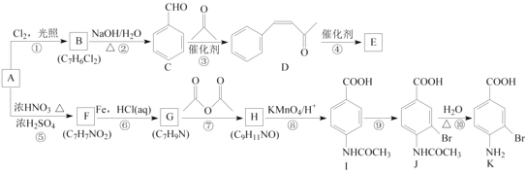
【题目】芳香烃A是基本有机化工原料,由A制备高分子E和医药中间体K的合成路线(部分反应条件略去)如下图所示:
己知:①![]() ;
;
②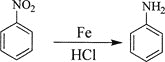
回答下列问题:
(1)A的名称是________,I含有官能团的名称是________。
(2)反应⑦的作用是________,⑩的反应类型是________。
(3)写出反应②的化学方程式:____________________________________________________。
(4)D分子中最多有________个原子共平面。E的结构简式为________。
(5)写出一种同时符合下列条件的F的同分异构体的结构简式:________。
①苯环上只有两种不同化学环境的氢原子;
②既能与银氨溶液反应又能与NaOH溶液反应。
(6)将由D为起始原料制备![]() 的合成路线补充完整。
的合成路线补充完整。
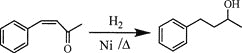 ________(无机试剂及溶剂任选)。
________(无机试剂及溶剂任选)。
合成路线流程图示例如下:
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置测定中和热的实验步骤如下:①用量筒量取50 mL 0.50 mol·L1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L1 NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
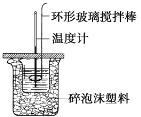
(1)使盐酸与NaOH溶液混合均匀的正确操作是___(填序号)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动。
(2)倒入NaOH溶液的正确操作是_____(填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)为什么所用NaOH溶液要稍过量?________。
(4)现将一定量的稀氢氧化钠溶液、浓氢氧化钙溶液、稀氨水分别和1 L 1 mol·L1的稀盐酸恰好完全反应,其热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的大小关系为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盖斯定律认为能量总是守恒的:化学反应过程一步完成或分步完成,整个过程的热效应是相同的。
已知:![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为达到预期的实验目的,下列操作中正确的有( )
①配制FeCl3溶液时,将FeCl3固体溶于盐酸中,然后再用水稀释到所需的浓度
②用10 mL的量筒量取4.80 mL的浓硫酸
③蒸发溶液时,边加热边搅拌,直至蒸发皿中的液体蒸干
④向无色溶液中加入BaCl2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,由此确定该溶液中一定含有SO![]()
⑤为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量
⑥中和热测定的实验中使用的玻璃仪器只有2种
⑦实验室可利用浓氨水和碱石灰混合的方法制取少量氨气
⑧除去NO中混有的NO2气体可通过水洗,再干燥后用向上排空气法收集
A. 5项 B. 4项
C. 3项 D. 2项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对古文献记载内容理解错误的是
A. 《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无沙黏土而为之”。“瓦”,传统无机非金属材料,主要成分为硅酸盐。
B. 《本草纲目》“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也”。这里所用的“法”是指蒸馏。
C. 《抱朴子·金丹篇》中记载:“丹砂烧之成水银,积变又还成丹砂”。该过程未发生氧化还原反应。
D. 《本草经集注》中关于鉴别硝石(KNO3)和朴硝(Na2SO4)的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了焰色反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应和反应类型不相符的是
A. 苯与浓硝酸、浓硫酸混合加热制取硝基苯(取代反应)
B. 在一定条件下,苯与氯气生成六氯环己烷(加成反应)
C. 由乙炔(![]() )制取氯乙烯(CH2=CHCl) (氧化反应)
)制取氯乙烯(CH2=CHCl) (氧化反应)
D. 在催化剂的作用下由乙烯制取氯乙烷(加成反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水漂白性的强弱,设计了如下的实验装置。
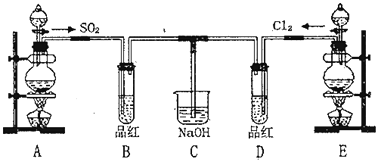
(1)实验室用装置A制备SO2.某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是_____
(2)实验室用装置E制备Cl2,写出反应的化学方程式_____请指出该反应中的液体反应物在反应中所表现出的化学性质_____。若液体反应物中的溶质反应了6mol,则标准状况下生成Cl2的体积为_____L
(3)停止通气后,再给BD两个试管分别加热,两个试管中的现象分别为:B_____、D_____
(4)C装置的作用是吸收尾气,防止污染空气,写出吸收Cl2的离子方程式_____
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通到品红溶液中,结果发现溶液基本不褪色。请你分析该现象的原因_____(用化学方程式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com