
【题目】有关下图装置中的叙述正确的是
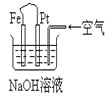
A.这是电解NaOH溶液的装置
B.这是一个原电池装置,利用该装置可长时间的观察到Fe(OH)2沉淀的颜色
C.Pt为正极,其电极反应为:O2+2H2O +4e-=4OH-
D.Fe为阳极,其电极反应为:Fe-2e-+2OH-=2Fe(OH)2
【答案】C
【解析】
碱性条件下,铁、铂丝和含有空气的氢氧化钠溶液构成原电池,铁发生吸氧腐蚀,铁作负极,负极上铁失电子发生氧化反应,铂丝作正极,正极上氧气得电子发生还原反应。
A.该装置没有外接电源,符合原电池的构成条件,所以该装置属于原电池,故A错误;
B.该装置属于原电池,发生铁的吸氧腐蚀,负极上电极反应式为Fe-2e-=Fe2+,正极上的电极反应式为:O2+2H2O+4e-=4OH-,亚铁离子和氢氧根离子反应生成氢氧化亚铁,过量空气会迅速氧化Fe(OH)2生成红褐色的Fe(OH)3,所以不能长时间观察Fe(OH)2沉淀的颜色,故B错误;
C.Pt为正极,正极上氧气得电子生成氢氧根离子,其电极反应为:O2+2H2O+4e-=4OH-,故C正确;
D.铁作负极,负极的电极反应式为Fe-2e-+2OH-=2Fe(OH)2,故D错误;
故答案选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组探究铜丝与足量浓硫酸的反应,装置(已略去夹持装置,其中铜丝可抽动)如图,下列有关说法不正确的是( )
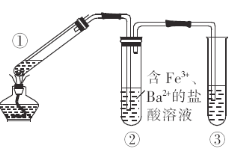
A.①中生成的气体可使品红溶液褪色
B.②中可观察到溶液黄色变浅,且有白色沉淀生成
C.为进行尾气处理,③中装有![]() 溶液
溶液
D.反应后,通过向①中加水,观察溶液颜色可判断反应有硫酸铜生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂与还原剂为同一种物质的是
A.SO2+2H2S=3S↓+H2B.2NO2+2NaOH=NaNO2+NaNO3+H2O
C.Zn+2HCl=ZnCl2+H2↑D.MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向一定体积的![]() 的
的![]() 溶液中逐滴加入
溶液中逐滴加入![]() 盐酸至过量,溶液中含碳元素的各微粒的物质的量浓度的百分含量随溶液pH的变化如图所示
盐酸至过量,溶液中含碳元素的各微粒的物质的量浓度的百分含量随溶液pH的变化如图所示![]() 因逸出未画出,滴加盐酸的过程中温度的变化忽略不计
因逸出未画出,滴加盐酸的过程中温度的变化忽略不计![]() 。下列说法正确的是
。下列说法正确的是![]()
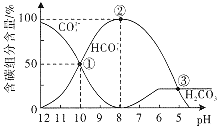
A.点![]() 时溶液中水的电离程度比纯水的大
时溶液中水的电离程度比纯水的大
B.点![]() 所示溶液中:
所示溶液中:![]()
C.当滴加盐酸到点![]() 时,才开始放出
时,才开始放出![]() 气体
气体
D.![]() 第一步水解反应的平衡常数:
第一步水解反应的平衡常数:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的△H前者小于后者的有( )
①C(s)+O2(g)═CO2(g) △H1 C(s)+![]() O2(g)═CO(g) △H2
O2(g)═CO(g) △H2
②S(s)+O2(g)═SO2(g) △H3 S(g)+O2(g)═SO2(g) △H4
③2H2(g)+O2(g)═2H2O(l) △H5 2H2(g)+O2(g)═2H2O(g) △H6
④CaCO3(s)═CaO(s)+CO2(g) △H7 CaO(s)+H2O(l)═Ca(OH)2(s) △H8
⑤![]() H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) ΔH9CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH10
Na2SO4(aq)+H2O(l) ΔH9CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH10
⑥N2O4(g)![]() 2NO2(g) △H11 2NO2(g)
2NO2(g) △H11 2NO2(g)![]() N2O4(g) △H12
N2O4(g) △H12
A.2项B.3项C.4项D.5项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.由三种元素组成的化合物 A,按如下流程进行实验:
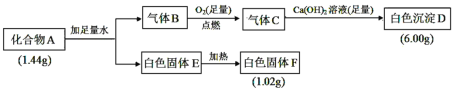
已知:①标准状况下,气体B的密度是氢气的8倍。②固体E既能溶于NaOH溶液又能溶于盐酸。
请回答:
(1)组成 A 的三种元素是__________,A 的化学式是________。
(2)固体 A 与足量稀盐酸反应的化学方程式是__________。
(3)气体 B 与足量 CuO 在加热条件下反应,请写出一个可能的化学方程式________________。
Ⅱ.某兴趣小组为探究 SO2 与 Fe(NO3)3 稀溶液反应的情况,实验装置如图,请回答:
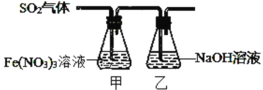
(1)实验过程中,甲中溶液由黄色变为浅绿色但立即又变为黄色。请写出甲中溶液由浅绿色变为黄色的离子方程式_____。
(2)请设计实验方案,检验反应后甲溶液中的金属阳离子______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用,其化合物也应用广泛。
(1)基态B原子的电子排布图为________________________,其第一电离能比Be___________(填“大”或“小”)。
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构简式为___________ (标出配位键),其中心原子的杂化方式为________,写出[BH4]-的一种阳离子等电子体_______。
(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为____________(以n表示硼原子的个数)。

(4)硼酸晶体是片层结构,下图表示的是其中一层的结构。每一层内存在的作用力有_________。

(5)三氯化硼的熔点比氯化镁的熔点低,原因是_______________________。
(6)镁单质晶体中原子的堆积模型如下图,它的堆积模型名称为_______;紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2a cm3,镁单质的密度为ρ g·cm-3,已知阿伏伽德罗常数为NA,则镁的摩尔质量的计算式是________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法不正确的是( )
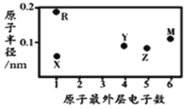
A.简单阳离子半径X最小
B.M的氢化物常温常压下为气体,分子间无氢键
C.最高价氧化物的水化物的酸性:Z<Y
D.X与Y可以形成平面形结构的分子,分子中存在极性共价键和非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙酸和乙醇在浓硫酸作用下可以发生加成反应
B.分子式为C4H9Cl的同分异构体有4种
C.甲醇、乙二醇、丙三醇互为同系物
D.聚乙烯塑料可用于食品的包装,该塑料的老化是由于发生了加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com