
【题目】固体氢氧化钠必须密封保存的原因是( )
①氢氧化钠有毒 ②氢氧化钠有腐蚀性 ③氢氧化钠易吸收水分而潮解 ④氢氧化钠有挥发性 ⑤氢氧化钠能与空气中的二氧化碳反应
A.①②B.②③④C.②③⑤D.③⑤
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.铁的摩尔质量就是铁的相对原子质量
B.SO42-的摩尔质量是96g/mol
C.1molO2的质量是32g/mol
D.CO2的摩尔质量是44g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A. 无色透明的溶液中:Fe3+、Mg2+、SCN–、Cl–
B. 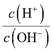 =1×10 12的溶液中:K+、Na +、CO32-、NO3-
=1×10 12的溶液中:K+、Na +、CO32-、NO3-
C. 浓度为3%的H2O2溶液:H+、Na+、C1-、SO32-
D. 能使甲基橙变红的溶液中:Na+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 金属钠加入到CuSO4溶液中:2Na+Cu2+===Cu+2Na+
B. 将铝片打磨后置于NaOH溶液中:2Al+2OH-===2AlO![]() +H2↑
+H2↑
C. 向明矾溶液中加入过量的Ba(OH)2溶液:Al3++2SO![]() +2Ba2++4OH- === 2BaSO4↓+AlO
+2Ba2++4OH- === 2BaSO4↓+AlO![]() +2H2O
+2H2O
D. 向Ba(AlO2)2溶液中通入少量CO2:2AlO![]() +CO2+3H2O===2Al(OH)3↓+CO
+CO2+3H2O===2Al(OH)3↓+CO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
(1)SO2(g)+2CO(g)2CO2(g)+S(l)△H<0
①如果要提高上述反应的反应速率,可以采取的措施是 . (选填编号)
a.减压 b.增加SO2的浓度 c.升温 d.及时移走产物
②若反应在恒容的密闭绝热容器中进行,下列说法不正确的是 . (选填编号)
a.平衡前,随着反应的进行,容器内压强始终不变
b.当容器内温度不再变化时,反应达到了平衡
c.其他条件不变,升高温度可增大平衡常数
d.其他条件不变,使用不同催化剂,该反应热效应不同
③该反应的平衡常数表达式是′;某温度下2L恒定容器中加入2mol的SO2和2mol的CO.10分钟内,气体密度减小了8g/L,则CO的反应速率是 .
(2)SO2(g)+NO2(g)NO(g)+SO3(g)
①在2L恒定容器中加入2mol的SO2和2mol的NO2 , 达到平衡时测得SO2的转化率为50%,向该容器中再加入1mol的SO2 , 平衡将向方向移动,计算重新达到平衡时SO2的浓度是 , SO2的转化率由50%变为 , NO2的转化率由变为 .
②实验结果启示我们:增大一种反应物浓度,其转化率将(填增大、减小或不变),另一种反应物的转化率将 . 现实生产的意义是:可以通过增大的用量,来提高成本高的反应物的利用率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种国际上公认的安全无毒的绿色水处理剂。回答下列问题:
(1)工业废水的处理:某实验兴趣小组通过下图装置,利用稀硫酸、KClO3和草酸溶液制备ClO2,并用它来处理含Mn2+的工业废水。

①A装置的名称是______________,C装置的作用为__________________。
②B中反应产物有ClO2、CO2等,请写出该反应的化学方程式:___________________。
③写出装置D中除去Mn2+的离子方程式__________________。(已知Mn2+转化为MnO2)
(2)ClO2易溶于水。用水吸收ClO2得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样:量取V1mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用cmol·L-1Na2SO3溶液滴定至终点,消耗Na2S2O3溶液V2mL。 (已知2Na2S2O3+I2=Na2S4O6+2NaI)
①滴定终点的判断依据是___________________。
②原ClO2溶液的浓度为_______________g/L(用步骤中的字母代数式表示)。
③若实验中使用的Na2S2O3标准溶液部分因被氧气氧化而变质,则实验结果___________(填“偏高”、“ 偏低”或“无影响”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com