
| A、原子半径Y>Z>W |
| B、Y氧化物属于酸性氧化物 |
| C、对应的氢化物的热稳定性:W>Z |
| D、X的最高价氧化物对应的水化物弱酸 |


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
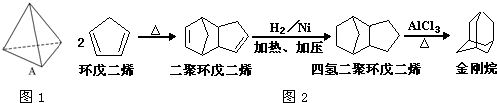
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢气在氯气中燃烧生成绿色烟雾 |
| B、碘水中加入少量汽油振荡静置后,下层液体为红色 |
| C、将无色的NO气体与空气混合时,看见气体变为红棕色 |
| D、向FeCl2溶液中滴入KSCN溶液,溶液变为血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、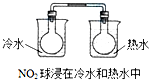 | ||||||||
B、
| ||||||||
C、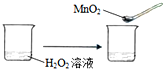 | ||||||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na与水反应时增大水的用量 |
| B、将稀H2SO4改为98%的浓H2SO4与Zn反应制取H2 |
| C、在H2SO4与NaOH两溶液反应时,增大压强 |
| D、恒温恒容条件下,在工业合成氨反应中,增加氮气的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
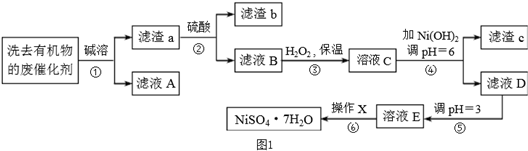
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
| 充电 |
| 放电 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L氢气所含原子数是2NA |
| B、5.4g水所含的分子数为0.3NA |
| C、1mol金属钠与水反应失去的电子数为NA |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | 过氧化钠 | |
| D | 吸收未反应的CO2气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com