
(12分)已知:2X(g)+Y(g) a Z(g),T1温度时,在体积为2L的密闭容器中充入6mol X和2 mol Y,根据图示回答:
a Z(g),T1温度时,在体积为2L的密闭容器中充入6mol X和2 mol Y,根据图示回答:

(1)a=__;用X的浓度变化表示从反应开始到平衡时的平均反应速率为 mol/(Lmin)。
(2)平衡时,Y在混合物中的物质的量分数是 。
(3)下列选项能说明反应达到平衡状态的是 (选填字母)。
A.容器内压强保持不变
B.容器内密度保持不变
C.X的物质的量不再变化
D.υ(X)正 =υ(Z)逆
(4)其他条件相同时,若升高温度到T2时,反应的平衡常数为1,下列措施可以提高Y的转化率的是 (选填字母)。
A.选择适当的催化剂 B.分离出Z
C.增大压强 D.升高温度
(5)X、Y、Z由C、H、O三种元素中的一种或几种组成,信息如下:
物质 | X | Y | Z |
所含元素种数 | 1 | 2 | 3 |
分子中的电子总数 | 大于10 | 18 | |
燃烧热(kJ/mol) | -285.8 | -283 | -726.5 |
①则Z的分子式为___________。
②根据燃烧热数据分析,等质量的X、Y、Z充分燃烧,放出热量最多的是__________(填分子式)。
(共12分)
(1)1;0.15mol/(Lmin)(各1分)
(2)0.1 (或1/10)
(3)A C
(4)BC
(5)①CH4O ②H2
【解析】
试题分析:(1)由反应浓度变化图可知,在10min时,Y浓度减小(1.0mol/L-0.25mol/L)=0.75mol/L,Z浓度增加0.75mol/L,所以a = 1;由方程式可知当Y浓度减小0.75mol/L时,X的浓度减小1.5mol/L,用X的浓度变化表示从反应开始到平衡时的平均反应速率为1.5mol/L/10min=0.15mol/(Lmin);(2)由三行式法可知平衡时,Y的物质的量为0.5mol,混合物的物质的量为5.0mol,Y在混合物中的物质的量分数是0.1 (或1/10);(3)A、该反应是一个体积减小的反应,当容器内压强保持不变时达平衡状态;B、由质量守恒,容器的体积不变,所以容器内密度始终保持不变;C、X的物质的量不再变化,达到平衡状态;D、当υ(X)正 =2υ(Z)逆时反应达平衡状态;答案选AC;(4)由浓度变化图像可知,温度为T1时,平衡常数为1.3,其他条件相同时,若升高温度到T2时,反应的平衡常数为1,可知该反应为放热反应;A、选择适当的催化剂,平衡不移动,Y的转化率不变;B、分离出Z,平衡向正方向移动,Y的转化率提高;C、增大压强,平衡向体积减小的方向移动,Y的转化率提高;D、升高温度,平衡向逆反应方向移动,Y的转化率减小;答案选BC;(5)由Y由两种元素组成,电子总数大于10,且燃烧热为-283kJ/mol,可知Y为CO;Z由3种元素组成,电子总数等于18,且燃烧热为-726.5kJ/mol,可知Z为CH4O;则X为H2 ;①则Z的分子式为CH4O;②根据燃烧热数据分析,等质量的X、Y、Z充分燃烧,放出热量最多的是H2。
考点:化学反应速率、化学平衡、反应热
考点分析: 考点1:化学平衡状态及移动 试题属性

科目:高中化学 来源:2014-2015学年山东省日照市高三3月模拟考试理综化学试卷(解析版) 题型:填空题
(16分)氢气是一种理想的“绿色能源”,利用氢能需要选择合适的储氢材料。目前正在研究和使用的储氢材料有镁系合金、稀土系合金等。

(2)储氢材料Mg(AlH4)2在110~200℃的反应为:Mg(AlH4)2==MgH2+2Al+3H2↑。
反应中每转移3mol电子时,产生的H2在标准状况下的体积为__________L。
(3)镧镍合金在一定条件下可吸收氢气形成氢化物:
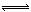 LaNi5H6(s)
LaNi5H6(s) ,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是_______(填字母编号)。
,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是_______(填字母编号)。
a.增加LaNi5H6(s)的量
b.升高温度
c.减小压强
d.使用催化剂
(4)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:

①某温度下,向恒容密闭容器中加入环己烷,起始浓度为amol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=____________(用含a、b的代数式表示)。
②一定条件下,下图装置可实现有机物的电化学储氢(忽略其它有机物)。

A是电源的______极(填“正”或“负”);电解过程中产生的气体F为_____(填化学式):电极D上发生的电极反应为__________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州五校高三上学期摸底联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.酸、碱、盐都是电解质 B.电解质都是易溶于水的物质
C.氧化物都是电解质 D.氢化物都不是电解质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三3月月考理综化学试卷(解析版) 题型:填空题
[化学一物质结构与性质)(13分)
I.镁条在空气中燃烧主要发生以下三个反应:
2Mg+O2 2MgO 3Mg+N2
2MgO 3Mg+N2 2Mg3N2 2Mg+CO2
2Mg3N2 2Mg+CO2 2MgO+C
2MgO+C
(1)基态氮原子核外电子的轨道表示式为 .
(2)上述三个反应中所涉及的非金属元素.的第一电离能由大到小的顺序为 。
(3)MgO的晶体结构模型如图所示,若MgO晶体密度为ρg/cm3,图示中O2-与O2-的核间距a= .

Ⅱ.Mg3N2溶于水发生反应:Mg3N2+8H2O=3Mg(OH)2↓+2NH3·H2O
(4)氨水中各种微粒间不涉及的作用力是 (填选项序号)。
A.离子键
B.共价键
C.配位键
D.金属键
E.氢键
F.范德华力
(5)在一定条件下将NH气与CO2混合可制得尿素[CO(NH2)2],尿素分子中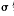 键的数目为 。
键的数目为 。
(6)向硫酸铜溶液中逐渐通入过量氨气,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。关于该晶体下列说法中正确的是 。
A.加入乙醇的目的是降低溶剂的极性,促使[Cn(NH3)4]SO4晶体析出
B.该配合物晶体中,N是配位原子,NH3为三角锥型,配位数是4
C.配离子内N原子排列成为平面正方形,可见Cu2+是sp3杂化
D.向该晶体的水溶液中加入浓BaCl2溶液有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三3月月考理综化学试卷(解析版) 题型:选择题
四种短周期元素在周期表中的相对位置如下图所示,其中Y为空气中含量最大的元素。下列叙述合理的是

A.元素W位于第三周期第ⅦA族
B.Y、Z都是植物必需的元素
C.原子半径:W>Z>Y>X
D.X氧化物的大量排放导致化学烟雾
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
实验:①0.1 mol/L AgNO3溶液和0.1 mol/L NaCl溶液等体积混合得到浊液,过滤。
②分别取少量①的滤液,分别滴加等浓度等体积的饱和Na2S溶液、饱和Na2SO4溶液,前者出现浑浊,后者溶液仍澄清。
③取少量①的沉淀,滴加几滴氨水,沉淀逐渐溶解。
下列分析不正确的是
A.实验②证明了①的滤液中含有Ag+,由此推断①的滤液中也含有Cl
B.实验②证明了该温度下Ag2S比Ag2SO4更难溶解
C.实验③的溶液中含有Ag(NH3)2+微粒
D.由实验③推测:若在①的沉淀中滴加NaOH溶液,沉淀也能溶解
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.HOCH2COOH的缩聚物是
B.乙醛和丙烯醛( )不是同系物
)不是同系物
C.已知甲醛分子中各原子共平面,则丙烯醛所有原子一定共平面
D.结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子的单体是1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省商丘市高三第一次模拟考试化学试卷(解析版) 题型:选择题
下列各表述与示意图不一致的是

A.图①表示向含Mg2+、Al3+、 的盐溶液中滴加NaOH溶液时,沉淀的物质的量与NaOH的体积的关系图。则三种离子的物质的量之比为:n(Mg2+) :n(Al3+) :n(
的盐溶液中滴加NaOH溶液时,沉淀的物质的量与NaOH的体积的关系图。则三种离子的物质的量之比为:n(Mg2+) :n(Al3+) :n( )=2 :1 :2,其中使用的NaOH的浓度为2 mol·L-1。
)=2 :1 :2,其中使用的NaOH的浓度为2 mol·L-1。
B.图②中曲线表示某反应过程的能量变化,当物质A(g)与B(g)反应生成物质C(g)时,△H<0,若使用正催化剂,E值会减小。
C.图③可用来表示向盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液时,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)之间的关系图
D.图④表示向一定质量的明矾溶液中滴加Ba(OH)2溶液时,产生沉淀的质量(m)与加入Ba(OH)2溶液体积(V)之间的关系图
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省文登市高三第二次统考理科综合化学试卷(解析版) 题型:选择题
下列关于离子的叙述正确的是
A.在c(H+)=1×10-13mol·L-1的溶液中:Na+、Fe3+、Cl-、SO42-能大量共存
B.铜溶于FeCl3溶液中:Cu + Fe3+ = Fe2+ + Cu2+
C.NaHCO3溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
D.向溶液中加入BaCl2溶液后再加盐酸,有白色沉淀,说明该溶液中一定含有SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com