
【题目】I、下面列出了几组物质:①金刚石与“足球烯”C60;②D2O与H2O;③16O、18O;④氧气与臭氧;⑤ 与
与 ;⑥CH3CH2CH2CH3和
;⑥CH3CH2CH2CH3和![]() ;⑦CH4和CH3CH2CH3;⑧CH3CH3和
;⑦CH4和CH3CH2CH3;⑧CH3CH3和![]() 。
。
其中互为同位素的是______;互为同素异形体的是_____;属于同系物的是_____;互为同分异构体______。
II、写出下列有机物的系统命名或结构简式:
(1)(CH3)2CH(CH2)2CH(C2H5)(CH2)2CH3_______。
(2)  _______。
_______。
(3) _____。
_____。
(4)2-甲基-2-丁烯_____________。
【答案】③ ①④ ⑦⑧ ⑥ 2-甲基-5-乙基辛烷 3,4-二甲基-2-戊醇 5-甲基-3-乙基-1-己炔 ![]()
【解析】
I关于“四同”的比较:
同位素:质子数相同中子数不同的核素;同素异形体:一种元素构成的不同物质,一定是单质;同分异构体:分子式相同,结构不同,必为化合物;同系物:结构相似,分子式相差若干CH2原子团。
II 判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:(1)烷烃命名原则:①长--选最长碳链为主链;②多--遇等长碳链时,支链最多为主链;③近--离支链最近一端编号;④小--支链编号之和最小;⑤简--两取代基距离主链两端等距离时,从简单取代基开始编号。如取代基不同,就把简单的写在前面,复杂的写在后面;含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小。
①金刚石与“足球烯”C60都是由碳元素形成的不同单质,互为同素异形体;
②D2O与H2O都是氢的同位素与氧元素形成的化合物;
③16O与18O质子数相同,中子数不同,互为同位素;
④氧气(O2)与臭氧(O3)都是由氧元素形成的不同单质,互为同素异形体;
⑤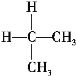 与
与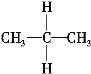 均为丙烷,属于同种物质;
均为丙烷,属于同种物质;
⑥CH3CH2CH2CH3和![]() 分子式相同,但结构不同,互为同分异构体
分子式相同,但结构不同,互为同分异构体
⑦CH4和CH3CH2CH3结构相似,分子组成相差2个“CH2”原子团,互为同系物,
⑧CH3CH3和![]() 结构相似,分子组成相差3个“CH2”原子团,故互为同系物;
结构相似,分子组成相差3个“CH2”原子团,故互为同系物;
即互为同位素的是③;互为同素异形体的是①④;属于同系物的是⑦⑧;互为同分异构体⑥ ;
答案: ③ ①④ ⑦⑧ ⑥
II (1)把碳链打开按照烷烃命名规则命名: ,最长的碳链含有8个C,主链为辛烷,编号从左边开始,取代基的编号最小,2号C一个甲基、5号C一个乙基,名称:2-甲基-5-乙基辛烷;
,最长的碳链含有8个C,主链为辛烷,编号从左边开始,取代基的编号最小,2号C一个甲基、5号C一个乙基,名称:2-甲基-5-乙基辛烷;
答案:2-甲基-5-乙基辛烷
(2)选择含有羟基的最长碳链为主链,从离羟基最近的一端开始编号,按照主链所含的碳原子数目称为"某醇";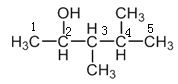 名称:3,4-二甲基-2-戊醇;
名称:3,4-二甲基-2-戊醇;
答案:3,4-二甲基-2-戊醇
(3)①首先选择含有碳碳三键的最长碳链作为主链,按主链中所含碳原子的数目命名为某炔;②给主链编号时从距离碳碳三键最近的一端开始,侧链视为取代基,碳碳三键的位次须标明;③其它同烷烃的命名规则;
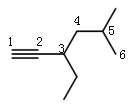 名称: 5-甲基-3-乙基-1-己炔;
名称: 5-甲基-3-乙基-1-己炔;
答案: 5-甲基-3-乙基-1-己炔
(4)2-甲基-2-丁烯,碳碳双键在2号C,甲基在2号C,主链为丁烯,结构简式为![]() ;
;
答案:![]()


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )
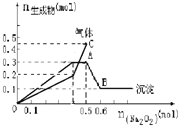
A. 1∶1∶2B. 2∶2∶1
C. 1∶2∶2D. 9∶2∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )

A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,通入HCl可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) TiO2是一种性能优良的半导体光催化剂,能有效地吸附有机污染物,Ti基态核外电子排布式为________________。
(2)甲醛HCHO分子空间构型为_____;分子中碳原子轨道杂化类型为_____,π键和σ键的个数之比为____,
(3)SO2易溶于水的原因是___________________________________。
(4)从原子结构角度解释H2SO4酸性强于H3PO4的原因:___________________________。
(5)含CN-的污水毒性极大,用NaClO先把CN-氧化为CNO-,然后在酸性条件下将CNO-氧化为无污染的气体。请写出与CNO-互为等电子体的微粒______(分子或离子,写一种)。
(6)下列物质在通常状况下的熔点由高到低的顺序为__________(填序号)
①CO ②Al2O3③NH3 ④N2⑤Br2
(7)不考虑空间构型,Ti[(CN)4]2-的结构可表示为:_____________________。
(8)向硫酸铜溶液中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,请根据实验现象写出有关反应的离子方程式 (1)____________________________(2)_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的有机产物,肯定是一种的是( )
A. 异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B. 2—氯丁烷(![]() )与NaOH溶液共热发生反应
)与NaOH溶液共热发生反应
C. 甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D. 等物质的量的甲烷和氯气的混和气体长时间光照后的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁的电化学腐蚀原理如图所示,下列有关说法中错误的是( )
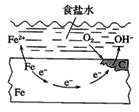
A. 铁片里的铁和碳与食盐水形成无数的微小原电池
B. 铁电极发生氧化反应
C. 负极的电极反应方程式为O2+4e-+2H2O=4OH-
D. 放置一段时间后,铁片上有铁锈出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为V L的恒容容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如下图所示。已知在反应过程中混合气体的总的物质的量没有变化。请回答:
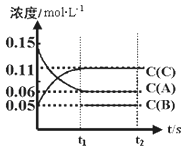
(1)V =_________。
(2)若t1=15s时,则0-t1阶段以C物质浓度变化表示的反应速率v(C)=__________。
(3)写出反应的化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知V是元素周期表中原子半径最小的原子。而W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。X 和 Ne 的核外电子数相差1,且 X和W能形成化合物X2W; 在Z所在的周期中,Z 元素的最高价氧化物的水化物酸性最强;四种元素的最外层电子数之和为18。 请回答下列问题:
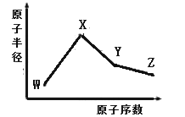
(1) Y元素位于元素周期表中位置为____________。
(2)已知U原子与V是同主族的短周期的元素,单核U、V离子具有相同的电子层结构,其离子的半径大小是:____________(写离子符号)
(3) Z的同族简单氢化物中,沸点最高的是________(写化学式),原因_______________________。
(4) W、X、Z 三种元素形成具有漂白性的化合物的电子式为___________;W的两种氢化物结构式分别为____________,______________。
(5) Y与Z形成的化合物YZ4在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2和NaClO2均具有漂白性,工业上用ClO2气体制NaClO2的工艺流程如图所示。
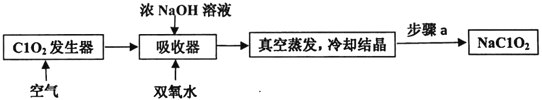
下列说法不正确的是
A. 步骤a的操作包括过滤、洗涤和干燥
B. 吸收器中生成NaClO2的离子方程式:2ClO2+H2O2=2C1O2-+O2↑+2H+
C. 工业上可将ClO2制成NaClO2固体,便于贮存和运输
D. 通入空气的目的是驱赶出ClO2,使其被吸收器充分吸收
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com