
【题目】聚苯乙烯塑料在生产、生活中有广泛应用,其单体可由乙苯和二氧化碳在一定条件下反应制得,其反应原理如下:

下列有关说法不正确的是
A. 苯乙烯可通过加聚反生成聚苯乙烯
B. 苯乙烯分子中所有原子可能共平面
C. 乙苯、苯乙烯均能使溴水褪色,且其褪色原理相同
D. 等质量的聚苯乙烯与苯乙烯中所含的碳原子数相同
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某同学设计了一个甲醇(CH3OH)燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图1:
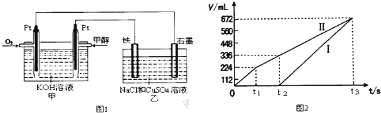
(1)25℃,1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为 。
(2)写出甲中通入甲醇这一极的电极反应式 。
(3)铁电极上反应的现象为:先有红色的物质析出,后 。
石墨电极上产生的气体是 。
(4)理论上乙中两极所得气体的体积随时间变化的关系如图2所示(气体体积已换算成标准状况下的体积)原混合溶液中CuSO4的物质的量浓度 mol·L-1。(假设溶液体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
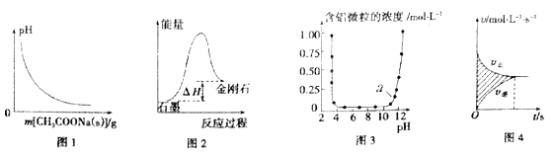
A. 图1表示向0.1mol/L CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B. 图2表示石墨转化为金刚石反应过程中的能量变化,可判断石墨比金刚石稳定
C. 图3表示Al3+与OH-反应时溶液中含铝微粒浓度变化曲线,图中a点溶液中大量存在Al3+
D. 图4表示某可逆反应的v-t曲线,图中阴影部分面积的含义是(v正-v逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用;锂元素更是被誉为“能源元素”。
Ⅰ、锂的原子结构示意图为___________;锂在空气中燃烧,发出浅蓝色的火焰,放出浓厚的白烟,生成相应氧化物____________(填化学式)。
Ⅱ、锂经常用于制作电池。锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:
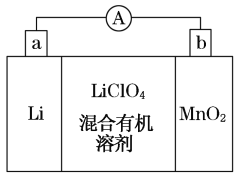
(1)外电路的电流方向是由________极流向________极。(填字母)
(2)电池正极反应式____________________________________。
(3)是否可用水代替电池中的混合有机溶剂?________(填“是”或“否”),用化学反应方程式解释原因______________________________________________。
Ⅲ、下面是从锂辉石(Li2O·Al2O3·SiO2)中提取锂的工业流程示意图。
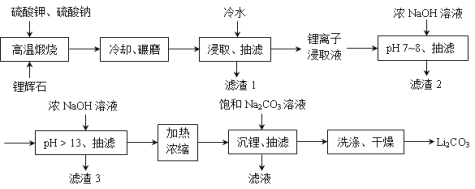
① 高温煅烧时的反应原理为:Li2OAl2O3SiO2+K2SO4= K2OAl2O3SiO2+Li2SO4;
Li2OAl2O3SiO2+Na2SO4= Na2OAl2O3SiO2+Li2SO4。
②锂离子浸取液中含有的金属离子为:K+、Na+、Li+、Fe3+、Fe2+、Al3+、Mn2+ 。
③几种金属离子沉淀完全的pH
金属离子 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 |
沉淀完全的pH | 4.7 | 9.0 | 3.2 | 10.1 |
④Li2SO4、Li2CO3在不同温度下的溶解度(g / 100g水)
温度 溶解度 | 10 | 20 | 50 | 80 |
Li2SO4 | 35.4 | 34.7 | 33.1 | 31.7 |
Li2CO3 | 1.43 | 1.33 | 1.08 | 0.85 |
(1)浸取时使用冷水的原因是______________________________________。
(2)滤渣2的主要成分为__________________。
(3)流程中分2次调节pH(pH7~8和pH > 13),有研究者尝试只加一次浓NaOH溶液使pH > 13,结果发现在加饱和碳酸钠溶液沉锂后,随着放置时间延长,白色沉淀增加,最后得到的Li2CO3产品中杂质增多。Li2CO3产品中的杂质可能是__________________,用离子方程式表示其产生的原因_____________________________。
(4)洗涤Li2CO3晶体使用_____________。(填“冷水”或“热水”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜在生活中有广泛的应用。CuCl2和CuCl是两种常见的盐,广泛应用于工业生产.
I.CuCl2固体遇水易水解。实验室用如图所示的实验仪器及药品来制备纯净、干燥的氯气,并与粗铜(含杂质铁)反应制备氯化铜(铁架台、铁夹及酒精灯省略)。
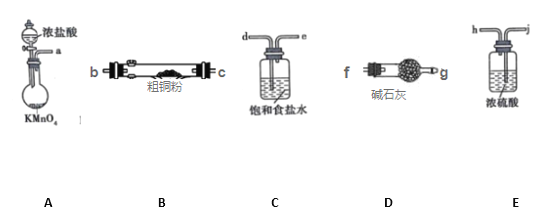
(1)写出装置A中,发生反应的化学反应方程式:_______________________________,装置C的作用是_______________________________
(2)完成上述实验,按气流方向连接各仪器接口的顺序是a→_________________________。(每种仪器限使用一次)
(3)上述D装置的作用是____________________
(4)实验完毕,取试管中的固体用盐酸溶解后,欲提纯氯化铜(原粗铜含杂质铁)可加入_________,并过滤。
A.Cu B.CuCO3 C.CuO D.NaOH
ⅡCuCl是应用广泛的有机合成催化剂,可采取不同方法制取。CuCl晶体呈白色,露置于潮湿空气中易被氧化。
方法一:向上述制得的氯化铜溶液中通入SO2,加热一段时间即可制得CuCl,写出该反应的离子方程式:_______________________________ 。
方法二 铜粉还原CuSO4溶液
![]()
已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+ 2Cl-![]() [CuCl3]2-(无色溶液)。
[CuCl3]2-(无色溶液)。
(1)①中,“加热”温度不宜过高和过低,目的是_______________,当观察到_________________________________________________________________________________现象,即表明反应已经完全。
(2)②中,加入大量水的作用是______________。(从平衡角度解释)
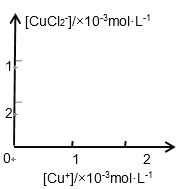
(3)溶液中氯离子浓度达到一定量时,生成CuCl会部分溶解生成CuCl2-在一定温度下建立两个平衡: Cu Cl(s)![]() Cu+(aq) + Cl-(aq) Ksp=1.4x10-6 Cu Cl(s) + Cl一(aq)
Cu+(aq) + Cl-(aq) Ksp=1.4x10-6 Cu Cl(s) + Cl一(aq)![]() CuCl2-(aq) K=0.35
CuCl2-(aq) K=0.35
分析[Cu+]、[CuCl2-]和Ksp,K的数学关系,在图中画出「Cu+]、[CuCl2-]的函数关系曲线(要求至少标出曲线上一个坐标点)
 _______________
_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂的保存或使用正确的是
A.实验室的氯水需要保存在棕色试剂瓶中
B.漂白粉比氯水稳定,可露置在空气中
C.称量氢氧化钠固体时,可在天平两个托盘上各放一张等质量的纸,左边纸上放NaOH,右边纸上放砝码
D.金属钠可保存在煤油、四氯化碳等有机溶剂中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200℃时,11.6gCO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体质量增加了3.6g,则原混合气体的平均摩尔质量为( )
A. 5.8g·mol-1 B. 11.6 g·mol-1
C. 23.2g·mol-1 D. 46.4g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4N3(叠氮化铵)易发生爆炸反应: NH4N3![]() 2N2↑+2H2↑,NA为阿伏加德罗常数的值,下列说法正确的是
2N2↑+2H2↑,NA为阿伏加德罗常数的值,下列说法正确的是
A. 1.8gNH4+中含有的质子数为1NA
B. N2既是氧化产物,又是还原产物
C. 爆炸反应中,当转移4NA个电子时,产生89.6L (标准状态)混合气体
D. 6g的NH4N3晶体中含有的阴离子个数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如右。下列说法不正确的是

A. 该过程将太阳能转化成为化学能
B. 该过程中,只涉及极性键的断裂与生成
C. 氧化剂与还原剂的物质的量之比为1∶3
D. 原料气N2可通过分离液态空气获得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com