
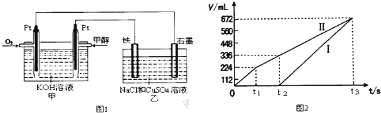
【题目】某同学设计了一个甲醇(CH3OH)燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图1:
(1)25℃,1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为 。
(2)写出甲中通入甲醇这一极的电极反应式 。
(3)铁电极上反应的现象为:先有红色的物质析出,后 。
石墨电极上产生的气体是 。
(4)理论上乙中两极所得气体的体积随时间变化的关系如图2所示(气体体积已换算成标准状况下的体积)原混合溶液中CuSO4的物质的量浓度 mol·L-1。(假设溶液体积不变)
【答案】(1)2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(l) ΔH=-1451.6KJ/mol
(2)CH3OH - 6e-+ 8OH- = CO32 -+ 6H2O
(3)有气泡产生 Cl2、O2
(4) 0.1
【解析】
试题分析:(1)16g液态甲醇完全燃烧,即16/32 =0.5mol的甲醇对应362.9kJ热量,据化学方程式,放出热量4x362.9=1451.6, 热化学方程式为2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(l) ΔH=-1451.6KJ/mol
(2)在燃料电池的中,负极上是燃料发生失电子的氧化反应,在碱性环境下,甲醇失电子的过程为:CH3OH-6e-+8OH-=CO32-+6H2O;
(3)石墨为阳极、铁电极为阴极,开始Cl-在阳极放电生成氯气,阴极Cu2+放电生成Cu,随着电解的继续,变成电解水放出氢气和氧气。
(4)图丙中Ⅰ表示阴极产生的气体,Ⅱ表示阳极产生的气体,t1前电极反应式为:阳极2Cl--4e-=Cl2↑,t2点后电极反应式为:阳极4OH--4e-=O2↑+2H2O,
由图可知,产生氯气为224mL,则由2Cl--2e-=Cl2↑可知,n(NaCl)=(0.224/22.4) ×2=0.02mol,所以c(NaCl)=0.02/0.2=0.1mol/L,
由t2时生成氧气为112mL,n(O2)=0.112/22.4=0.005mol,则共转移电子为0.02mol+0.005mol×4=0.04mol,
根据电子守恒及Cu2++2e-=Cu可知,n(CuSO4)=0.04mol/2=0.02mol,所以c(CuSO=0.02mol/0.2L=0.1mol/L,


科目:高中化学 来源: 题型:
【题目】全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色。下列叙述正确的是
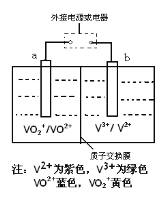
A.充电时右槽溶液颜色由紫色变为绿色
B.放电时,b极发生还原反应
C.充电过程中,a极的反应式为:VO2++2H++e—= VO2+ +H2O
D.电池的总反应可表示为:VO2++V2++2H+ ![]() VO2++V3++H2O
VO2++V3++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着我国汽车年销量的大幅增加,给空气环境造成了很大的污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )

A. 反应中NO为氧化剂,N2为氧化产物
B. 汽车尾气的主要污染成分包括CO、NO和N2
C. NO和O2必须在催化剂表面才能反应
D. 催化转化总化学方程式为2NO+O2+4CO ![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的溶液中,能大量共存的离子组是
A.Na+、Mg2+、H+、OH-B.H+、Al3+、AlO2-、CO32-
C.H+、Fe3+、Cl-、SiO32-D.K+、Ca2+、NO3-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将红热的固体单质M放入浓硝酸中,剧烈反应,产生混合气体A,A在常温下不与空气接触时,发生如图所示的变化。

(1)混合气体A的主要成分是____________。
(2)气体B为__________,蓝色溶液D为____________。
(3)单质M与浓硝酸反应的化学方程式是____________________________。
(4)单质C与稀硝酸反应的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法正确的是( )
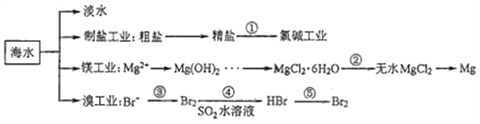
A. 海水淡化的方法主要有蒸馏法、电渗析法、冰冻法
B. 氯碱工业中采用阴离子交换膜可提高产品的纯度
C. 由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干
D. 溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯塑料在生产、生活中有广泛应用,其单体可由乙苯和二氧化碳在一定条件下反应制得,其反应原理如下:

下列有关说法不正确的是
A. 苯乙烯可通过加聚反生成聚苯乙烯
B. 苯乙烯分子中所有原子可能共平面
C. 乙苯、苯乙烯均能使溴水褪色,且其褪色原理相同
D. 等质量的聚苯乙烯与苯乙烯中所含的碳原子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com