
ЎѕМвДїЎїПВБРОпЦКµД·ЦАаХэИ·µДКЗ
СЎПо | јо | Лб | СО | јоРФСх»ЇОп | ЛбРФСх»ЇОп |
A | Na2CO3 | H2SO4 | Cu(OH)2CO3 | Fe2O3 | SO3 |
B | NaOH | HCl | NaCl | Na2O | CO |
C | NaOH | NaHSO4 | CaF2 | MgO | SO2 |
D | KOH | HNO3 | NaHCO3 | CaO | CO2 |
 Мб·Ц°Щ·Ц°ЩјмІвѕнПµБРґр°ё
Мб·Ц°Щ·Ц°ЩјмІвѕнПµБРґр°ё ±¦±ґјЖ»®ЖЪД©іеґМ¶б100·ЦПµБРґр°ё
±¦±ґјЖ»®ЖЪД©іеґМ¶б100·ЦПµБРґр°ё ДЬїјКФИ«ДЬ100·ЦПµБРґр°ё
ДЬїјКФИ«ДЬ100·ЦПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїИзНјОЄ·ґУ¦2H2ЈЁgЈ©Ј«O2ЈЁgЈ©===2H2OЈЁgЈ©µДДЬБї±д»ЇКѕТвНјЈ¬ПВБРЛµ·ЁґнОуµДКЗ

AЈ®ІрїЄ2molH2ЈЁgЈ©єН1molO2ЈЁgЈ©ЦРµД»ЇС§јь№ІОьКХ1368kJДЬБї
BЈ®УЙHЎўOФЧУРОіЙ2molH2OЈЁgЈ©Ј¬№І·Еіц1852kJДЬБї
CЈ®1molH2ЈЁgЈ©єН1/2molO2ЈЁgЈ©·ґУ¦ЙъіЙ1molH2OЈЁlЈ©Ј¬·ЕіцИИБїРЎУЪ242kJ
DЈ®2molH2ЈЁgЈ©єН1molO2ЈЁgЈ©·ґУ¦ЙъіЙ2molH2OЈЁgЈ©Ј¬№І·Еіц484kJИИБї
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї¶ФAlЎўFe¶юЦЦЅрКфФЄЛШЈ¬ПВБРЛµ·ЁХэИ·µДКЗ
A. ВБДЬ№»ОИ¶ЁґжФЪУЪїХЖшЦРЈ¬¶шМъєЬИЭТЧЙъРвЈ¬ЛµГчМъ±ИВБ»оЖГ
B. µИОпЦКµДБїµДAlЎўFe·Ц±рУлЧгБїСОЛб·ґУ¦·ЕіцµИЦКБїµДH2
C. ¶юХЯµДЗвСх»ЇОп¶јІ»їЙТФНЁ№эСх»ЇОп»ЇєП·ґУ¦Ц±ЅУЦЖ±ё
D. ¶юХЯµДµҐЦК¶јДЬУлЗїјоИЬТє·ґУ¦ЙъіЙH2
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРКфУЪСх»ЇОпµДКЗ
A. HNO3 B. NO2 C. NaNO3 D. Al(OH)3
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїИЎ50mLµДNa2CO3єНNa2SO4 µД»мєПИЬТєЈ¬јУИлККБїBa(OH)2ИЬТє50mLєуЈ¬ЗЎєГНкИ«·ґУ¦Ј¬№эВЛµГµЅВЛТєєН12.54g°ЧЙ«іБµнЈЁёЙФпєуЈ©Ј¬ФЩУГЧгБїµДПЎПхЛᴦАніБµнЈ¬ЧоєуіБµнјхЙЩµЅ4.66gЈ¬ІўУРЖшМе·ЕіцЎЈ
ЈЁ1Ј©4.66g°ЧЙ«іБµнКЗ_________ЈЁМо»ЇС§КЅЈ©Ј¬Рґіц12.54g°ЧЙ«іБµнјУИлПЎПхЛбєу±дОЄ4.66gЛщ·ўЙъ·ґУ¦µДАлЧУ·ЅіМКЅ___________________________Ј»
ЈЁ2Ј©ІъЙъµДЖшМеФЪ±кЧјЧґїцПВµДМе»эОЄ__________mlЈ»
ЈЁ3Ј©Ф»мєПТєЦРNa2SO4µДОпЦКµДБїЕЁ¶И______Ј»
ЈЁ4Ј©јЖЛг№эВЛіц12.54gіБµнєуЈ¬ЛщµГВЛТєЦРИЬЦКµДОпЦКµДБїЕЁ¶ИЈЁєцВФ»мєПИЬТєМе»эµД±д»ЇЈ©______ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДіРЛИ¤РЎЧйЙијЖСРѕїНєНПЎПхЛб·ґУ¦ЛЩВКVЈЁNOЈ©µДКµСйЎЈКФ»ШґрПВБРОКМвЈє
ЈЁ1Ј©РґіцНєНПЎПхЛб·ґУ¦µДАлЧУ·ЅіМКЅ___________________ЎЈ
ЈЁ2Ј©ОЄІв¶ЁНєНПЎПхЛб·ґУ¦ЛЩВКvЈЁNOЈ©Ј¬±ѕКµСйРиТЄјЗВјµДКµСйКэѕЭОЄЈє______________Ўў___________ЎЈ
ЈЁ3Ј©ёГРЛИ¤РЎЧйјдС§¶ФКµСйКэѕЭЅшРРґ¦АнєуµГµЅУГNO±нКѕНєНПЎПхЛбµД·ґУ¦ЛЩВКєНК±јдµД№ШПµНјИзНјЛщКѕ.„tЈє
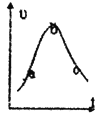
aЎЄbЈ¬vЈЁNOЈ©±д»ЇµДЦчТЄФТтКЗ___________________ЎЈ
bЎъcЈ¬vЈЁNOЈ©±д»ЇµДЦчТЄФТтКЗ___________________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЅ«MgМхН¶ИлКўУРПЎHClµДИЭЖчАпЈ¬ІъЙъH2µДЛЩВКУлПВБРТтЛШУР№ШПµµДКЗ( )
ўЩСОЛбЕЁ¶И ўЪОВ¶И ўЫГѕМхµД±нГж»э ўЬИЭЖчµДГЬ±ХЗйїц ўЭИЬТєЦРc(Cl-)ґуРЎ
AЈ®ўЩўЪ BЈ®ўЫўЬ CЈ®ўЩўЪўЫ DЈ®ўЩўЪўЫўЬўЭ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїОЄБЛід·ЦАыУГНЧКФґЈ¬Ді№¤і§ДвУГ»ЖН»Т(є¬УРCuЎўZnЎўCuOЎўZnOј°ЙЩБїµДFeOЎўFe2O3ЎўSiO2µИ)ЦЖИЎЅрКфНІўµГё±ІъОпРїСОЈ¬ЖдЙъІъБчіМИзПВЈє
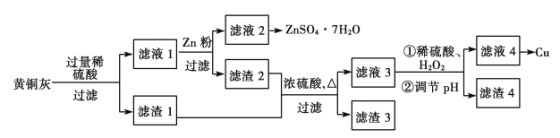
(1)ВЛФь1µДЦчТЄіЙ·ЦОЄ__________ЎЈПЎБтЛбИЬЅв»ЖН»Т№эіМЦРЈ¬їЙДЬ·ўЙъ¶аёцСх»Ї»№Ф·ґУ¦Ј¬ЖдЦРГ»УРZnІОјУµД·ґУ¦µДАлЧУ·ЅіМКЅКЗ_______________________
(2)ВЛФь1ј°ВЛФь2УГЕЁБтЛбЅюИЎїЙДЬІъЙъµДУР¶ѕЖшМеКЗ________Ј¬КµСйКТНЁіЈУГ__________ИЬТєОьКХЎЈ
(3)ПЎБтЛбНЁ№эЕЁБтЛбПЎКНµГµЅЈ¬ПЎКНЕЁБтЛбµДХэИ·ІЩЧч·Ѕ·ЁКЗ_____________________ЎЈ№эВЛІЩЧчЛщРиІЈБ§ТЗЖчіэІЈБ§°фНв»№УР_______________________
(4)УГ¶иРФµзј«µзЅвВЛТє4їЙЦЖИЎЅрКфНЈ¬ИфЦЖµГЅрКфН12.8 gЈ¬ФтН¬К±Сфј«µГµЅ______LЖшМе(±кЧјЧґїц)ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРОпЦКРФЦКУлУ¦УГ¶ФУ¦№ШПµХэИ·µДКЗ
A. MnO2І»ИЬУЪЛ®Ј¬їЙУГЧчH2O2·ЦЅвµДґЯ»ЇјБ
B. №эСх»ЇёЖCaO2»єВэУлЛ®·ґУ¦ДЬІъЙъO2Ј¬їЙУГЧчЛ®ІъСшЦіЦРµД№©СхјБ
C. ѕ§Ме№иИЫµгёЯУІ¶ИґуЈ¬їЙУГУЪЦЖЧч°лµјМеІДБП
D. Al(OH)3ѕЯУРБЅРФЈ¬їЙУГУЪЧцЧиИјјБ
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com