
有8 g Na2O2、Na2O、Na2CO3、NaOH的混合物与200 g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体质量为( )
A.8 g B.15.5 g C.11.7 g D.无法计算
科目:高中化学 来源:2014年化学高考总复习课时演练 4-3硫及其重要化合物练习卷(解析版) 题型:实验题
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
【探究一】
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________________。
(2)另取铁钉6.0 g放入15.0 mL浓硫酸中,加热,充分反应后收集到气体Y。
甲同学取336 mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为______。
【探究二】
分析上述实验中SO2体积分数的结果,乙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。

(3)装置B中试剂的作用是_________________________________________。
(4)认为气体Y中还含有Q的理由是______________________________。(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于______(选填序号)。
a.A之前 b.A、B间 c.B、C间 d.C、D间
(6)如果气体Y中含有H2,预计实验现象应是____________________________。
(7)若要测定限定体积气体Y中H2的含量(标准状况下约有28 mL H2),除可用测量H2体积的方法外,可否选用质量称量的方法?做出判断并说明理由________。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 3-3铁及其重要化合物练习卷(解析版) 题型:填空题
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:
①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;
B+H能放出大量的热,该反应曾应用于铁轨的焊接;
②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中E元素的质量分数为60%。
2F+D,F中E元素的质量分数为60%。

回答问题:
(1)①中反应的化学方程式为:________________________________________;
(2)1.6 g G溶于盐酸,得到的溶液与铜粉完全反应,计算至少需铜粉的质量(写出离子方程式和计算过程);__________________________________________。
(3)C与过量NaOH溶液反应的离子方程式为:___________________________,反应后溶液与过量化合物I反应的离子方程式为:_________________________;
(4)E在I中燃烧观察到的现象是:____________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 3-2铝及其重要化合物练习卷(解析版) 题型:选择题
用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是
( )
①加盐酸溶解
②加烧碱溶液溶解
③过滤
④通入过量CO2生成Al(OH)3沉淀
⑤加入盐酸生成Al(OH)3沉淀
⑥加入过量烧碱溶液
A.①⑥⑤③ B.②③④③ C.②③⑤③ D.①③⑤③
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 3-1钠及其重要化合物练习卷(解析版) 题型:实验题
一般测定样品中成分含量的实验应重复2~3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙、丙三位同学分别设计了如下实验方案:

Ⅰ.甲同学的方案如图所示:
(1)如何检验A装置的气密性?_____________________________________________。
(2)甲同学重复进行了三次实验,得到碳酸钠的质量分数的数据存在较大的偏差,你认为可能引起测量结果偏低的原因是_______(填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收
D.加入稀硫酸的量不足、反应不充分
(3)为了让甲的实验测量结果更准确,在其他实验步骤都正确的条件下,你认为图中的实验装置应该如何改进:______________。
Ⅱ.乙同学的方案是:从图中所提供的装置中选择实验装置,代替甲同学实验装置中的B、C,通过测定放出的二氧化碳的体积(不考虑二氧化碳溶于水)来计算。

选择最简装置的连接顺序为_______。
Ⅲ.丙同学的方案是:称取样品m g,并溶解,加入过量氯化钡溶液,过滤、洗涤、烘干、称量,得固体n g。
(1)配制100 mL 0.10 mol/L BaCl2溶液的实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外还有_______(填仪器名称)。
(2)混合物中碳酸钠的质量分数为(用m、n表示)_______。
(3)Ca2+、Ba2+都可以使 沉淀完全,能否使用氯化钙溶液代替氯化钡溶液?_______ (填“能”或“否”),原因是:_____________________________________。
沉淀完全,能否使用氯化钙溶液代替氯化钡溶液?_______ (填“能”或“否”),原因是:_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 3-1钠及其重要化合物练习卷(解析版) 题型:选择题
下列推断正确的是( )
A.等质量的NaHCO3和Na2CO3固体中,分别加入足量盐酸,NaHCO3产生的气体多
B.Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C.乙醇与金属钠的反应比水与金属钠的反应平缓得多,说明乙醇羟基中的氢原子比水分子中的氢原子活泼
D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液最终呈红色
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 2-3氧化还原反应练习卷(解析版) 题型:选择题
亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害。其在酸性条件下会产生NO和NO2。下列有关说法错误的是( )
A.NaNO2既具有氧化性又具有还原性
B.食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害
C.NaNO2和胃酸作用的离子方程式为: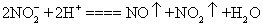
D.1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 2-2离子反应练习卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.将Na投入CH3COOH中:2Na+2H+=2Na++H2↑
B.将过量氨水加入到AlCl3溶液中:Al3++4OH-=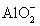 +2H2O
+2H2O
C.向氯化银悬浊液中加入溴化钾溶液:Ag++Br-=AgBr↓
D.碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液:Ca2++ 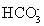 + OH-= CaCO3↓+H2O
+ OH-= CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 11-3物质的制备练习卷(解析版) 题型:选择题
有如下几种制备气体的方案:
①用稀硝酸与锌粉反应制氢气;②用水与过氧化钠固体反应制氧气;③常温下用铁片和浓硫酸制备二氧化硫;④氧化钙与浓氨水反应制氨气。不宜采用的方案有( )
A.①③ B.②③ C.③④ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com