
【题目】实验室中常用到0.1 mol/L的NaOH溶液,其中的“mol/L”对应的物理量是( )
A. 体积B. 物质的量浓度C. 摩尔质量D. 质量分数
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,请回答有关问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为 ________ ;
(2)表中能形成两性氢氧化物的元素是 ________ (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式:_________;
(3)③⑦⑩三种元素的阴离子还原性顺序为: _________________;⑦单质的水溶液呈__________色;
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 _______(填物质化学式) ;(提示:同周期元素,从左到右非金属性逐渐增强。)
(5)③元素与⑩元素两者核电荷数之差是 ____________ ;
(6)设计实验方案:比较⑦与⑥单质氧化性的强弱,请将方案填入下表。
实验步骤 | 实验现象与结论 |
____________________ | ____________________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2![]() 2SO3并达到平衡。若在这一过程中,甲容器保持体积不变,乙容器保持压强不变,则关于甲、乙两容器说法正确的是( )
2SO3并达到平衡。若在这一过程中,甲容器保持体积不变,乙容器保持压强不变,则关于甲、乙两容器说法正确的是( )
A. 达平衡时间甲比乙短
B. 乙容器中再充入等物质的量的SO2和O2,重新达平衡时转化率减小
C. 达平衡时,甲中SO2的浓度比乙中SO2的浓度大
D. 达平衡时,甲的转化率比乙低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由物质a为原料,制备物质d(金刚烷)的合成路线如下图所示:
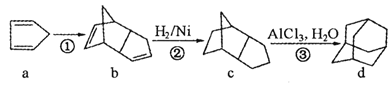
关于以上有机物的说法中,不正确的是
A. a分子中所有原子均在同一平面内 B. a和Br2按1:1加成的产物有两种
C. d的一氯代物有两种 D. c与d的分子式相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、G六种元素均为前四周期元素,原子序数依次增大。A原子核外的L层电子数是K层的两倍;C原子核外的最外层中只有两对成对电子,D在元素周期表的各元素中电负性最大,E和C同主族,G是前四周期元素中基态原子未成对电子数最多的元素。
请回答下列问题:
(1)A、B、C的第一电离能从小到大的顺序为_______。(用元素符号表示)
(2)AC2与EC2分子的空间构型分别是_______和_______。相同条件下EC2在水中的溶解度比AC2更大,理由是_______。
(3)用氢键表示式写出D的氢化物在水溶液中存在的任意一种氢键_______。
(4)G的价电子排布式为_______;G与CO形成的配合物G(CO)6中,1molG(CO)6中含有的σ键数目为_________。
(5)和G同周期的铁元素,其单质及其化合物应用广泛。
①某有机铁肥[Fe(H2NCONH2)6](NO3)3的名称叫三硝酸六尿素合铁,是一种配合物。该配合物中所含的阴离子的空间构型为_____,写出一个与该阴离子互为等电子体的分子________。
②氯化亚铁的熔点为674℃,而氯化铁的熔点仅为282℃,二者熔点存在差异的主要原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中,非金属元素集中于右上角的位置,它们虽然种类少,但其用途却不容小觑。
(1)元素周期表的非金属元素中,属于主族元素的共有________种。
(2)红磷是巨型共价分子、无定型结构。能证明红磷是非晶体的最可靠方法是________。
A.质谱 B.原子发射光谱 C.核磁共振谱 D.X射线衍射
(3)成语“信口雕黄”中的雌黄分子式为As2S3,分子结构如右图。
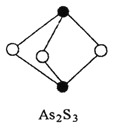
其分子中S原子的杂化方式为________。雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,写出该反应的化学方程式______。
(4)已知pKa=-lgKa。
①有机酸的酸性强弱受邻近碳上取代原子的影响,如酸性:BrCH2COOH>CH3COOH。据此推测,pKa:ClCH2COOH______FCH2COOH(填“>”、“<”、“=”)。
②硼酸(H3BO3)是一元酸,它在水中表现出来的弱酸性,并不是自身电离出H+所致,而是H3BO3与水电离出的OH-结合生成一个酸根离子,请写出该酸根离子的结构简式: ________(若存在配位键,请用箭头标出)。
(5)磷化硼的晶胞模型如右图所示,晶胞参数为apm,已知B、P的原子半径分别表示为rBpm、rPpm。该晶胞中磷原子的配位数为________,晶体中原子的空间利用率为______。
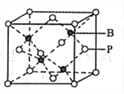
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将某些化学知识用图象表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,不正确的是( )
A. 分散系分类 ![]()
B. 醋酸稀释 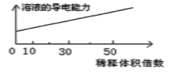
C. 向碳酸钠溶液中逐滴加入盐酸 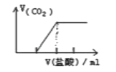
D. 向氯化铝溶液中滴加过量的NaOH溶液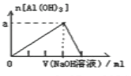
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 放热反应一定不需要加热
B. 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
C. 使用催化剂不但能加快反应速率,而且可以让不可能发生的反应发生
D. 难溶物也可能是强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F六种主族元素,A、B同周期相邻,A、C同主族相邻,A、B、C三种元素的原子序数之和为31,D元素与A、B、C三种元素既不同周期也不同主族,但D单质与A、B、C单质均可以反应,E是短周期主族中原子半径最大的元素,F是B同周期相邻元素。回答下列问题:
(1)写出C的元素符号:_______________ D在周期表中的位置____________________ 。
(2)B、D可直接化合生成化合物x, x分子与A、D形成的分子的稳定性比较_____________________________。(用化学式表示)
(3)A、B、D可组成离子化合物y的化学式为__________;E与C按1:1形成的化合物的电子式为____________ 。
(4)A、C形成的一种既有氧化性又有还原性的常见化合物,它对环境的影响之一是__________________________。
(5) 标准状况下9g F与A的单质完全燃烧产生的气体通入到1 L 1 mol·L-1的NaOH 溶液中,完全反应后溶液中存在的主要离子是_____________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com