
����Ŀ��HecK��Ӧ��ż����Ӧ��һ�֣����磺![]() +
+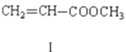
![]()
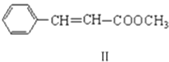 ��������������������;���ϳɣ���(����ʽC3H6)
��������������������;���ϳɣ���(����ʽC3H6)![]() ��
��![]() ��
��![]() I
I
(1)���������ķ���ʽΪ_______��1mol������������________molH2�����ӳɷ�Ӧ��
(2)±����CH3CHBrCH3������ȥ��Ӧ�������ɻ�����������Ӧ�Ļ�ѧ����Ϊ_______(ע������)��
(3)�����������м�����֧����ͬϵ�����ķ���ʽΪC4H6O���������Ľṹ��ʽΪ____��
(4)������������CH3CH2OH����������Ӧ���ɻ�������������������һ�������¿��Է����Ӿۣ�����Ӿ۲���Ľṹ��ʽΪ_____��
(5)����������һ��ͬ���칹�����ܷ���������Ӧ���Һ˴Ź�������ֻ������壬�����֮��Ϊ1:2:2�����Ľṹ��ʽΪ____��
(6)һ�������£�![]() ��
��![]() Ҳ���Է������Ʒ�Ӧ�ٵķ�Ӧ�����л�����Ľṹ��ʽΪ_____��
Ҳ���Է������Ʒ�Ӧ�ٵķ�Ӧ�����л�����Ľṹ��ʽΪ_____��
���𰸡�C10H10O2 4 CH3CHBrCH3+NaOH![]() CH2=CHCH3+NaBr+H2O CH3CH=CHCHO
CH2=CHCH3+NaBr+H2O CH3CH=CHCHO ![]()
![]()
![]()
��������
ͨ�������Ľṹ��ʽ�ķ�����֪��C3H6Ϊ��ϩ����CH3CH=CH2���ӷ�Ӧ������֪����������ȩ���������ķ�Ӧ����֪����ΪCH2=CHCHO����ΪCH2=CHCOOH���ݴ˷������
(1)ͨ�����Ľṹ��ʽ���ɵ������ʽΪC10H10O2�����������������ӳɣ�ֻ�б�����̼̼˫�������������ӳɣ�����1mol������������4mol���������ӳɷ�Ӧ���ʴ�Ϊ��C10H10O2��4��
(2)±������ȥ��Ӧ��������NaOH���Ҵ���Һ���ȣ������䷴Ӧ����ʽΪCH3CHBrCH3+NaOH![]() CH2=CHCH3+NaBr+H2O���ʴ�Ϊ��CH3CHBrCH3+NaOH
CH2=CHCH3+NaBr+H2O���ʴ�Ϊ��CH3CHBrCH3+NaOH![]() CH2=CHCH3+NaBr+H2O��
CH2=CHCH3+NaBr+H2O��
(3)��������ΪCH2=CHCHO���京�м�����֧����ͬϵ����ֻ����CH3CH=CHCHO���ʴ�Ϊ��CH3CH=CHCHO��
(4))��ΪCH2=CHCOOH������CH3CH2OH����������Ӧ���ɻ�����������ΪCH2=CHCOOCH2CH3���䷢���Ӿ۷�Ӧʱ����̼̼˫���ļӾۣ�����Ϊ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(5)���������Ľṹ��ʽΪ![]() ����ͬ���칹�����ܷ���������Ӧ������ȩ�����Һ˴Ź�������ֻ������壬�����֮��Ϊ1:2:2�����������ֵ�Ч���Ҹ�����Ϊ1:2:2�������������������Ľṹ��ʽΪ
����ͬ���칹�����ܷ���������Ӧ������ȩ�����Һ˴Ź�������ֻ������壬�����֮��Ϊ1:2:2�����������ֵ�Ч���Ҹ�����Ϊ1:2:2�������������������Ľṹ��ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(6)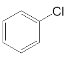 ��
��![]() Ҳ���Է������Ʒ�Ӧ�ٵķ�Ӧ��
Ҳ���Է������Ʒ�Ӧ�ٵķ�Ӧ�� ��Clԭ�ӱ�
��Clԭ�ӱ�![]() ȡ�������л�����Ľṹ��ʽΪ
ȡ�������л�����Ľṹ��ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)A��B��C��D��E��X����ѧ���������������ͼת����ϵ������������ͷ�Ӧ������ȥ����
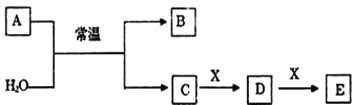
����AΪ�����Ľ������ʣ���ɫ��Ӧ�ʻ�ɫ��X��ʹƷ����Һ��ɫ��д��C��E��Ӧ�����ӷ���ʽ��___________________��
����AΪ����ɫ��ĩ��XΪһ��������������ЧӦ�����塣������Ũ�ȵ�D��E����ϡ��Һ����ѡ����Լ�Ϊ_________������ţ���
a������ b��BaCl2��Һ c��Ca(OH)2��Һ
����AΪ�ǽ��������BΪ���壬������������ɫ��X��Fe����ҺD�м���KSCN��Һ��졣��A��H2O��Ӧ�Ļ�ѧ��Ӧ����ʽ________________��
��2�����⻯�����������������ж�����Ҫ��;����⻯����ҽ�Ƽ�ʳƷ��������Ҫ�����ã�ʵ������NaOH�����ʵ��ˮ����(N2H4��H2O)Ϊԭ���Ʊ��⻯�ơ�ˮ���£����л�ԭ�ԣ����Ʊ��йط�Ӧԭ��Ϊ�� CO(NH2)2(����)+NaClO+2NaOH![]() N2H4��H2O+NaCl+Na2CO3
N2H4��H2O+NaCl+Na2CO3
����ȡ�������ƺ��������ƻ��Һ������˳��Ϊ__________(������������Сд��ĸ��ʾ)��B��D��װ�ֱ�װ���Լ���____________
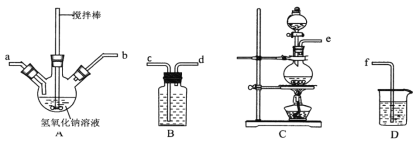
����ʵ���¶ȿ��Ʋ�������Ӧ��������ƿ��ClO-��ClO3-�����ʵ���֮��Ϊ5��1��������������������Ӧʱ������ԭ����Ԫ���뱻��������Ԫ�ص����ʵ���֮��Ϊ________��
���Ʊ�ˮ����ʱ��Ӧ��___________�ε� __________ �У�����NaClO��Һ������������Һ�������ҵμ��ٶȲ��ܹ��졣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.ij C3H6 ������ֻ��һ���⣬˵�����л���Ϊ��ϩ
B.��ϩ��ʹ��ˮ��ɫ��˵����ϩ����Ư����
C.���������������ӳɷ�Ӧ��˵���������к���̼̼˫��
D.�ױ����γ� 2,4,6-�������ױ����������γ� 1,3,5-����������˵�����Ա�����Ӱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϲ��ؾ��п��������ס��������������������á����Ľṹ��ʽ��ͼ��ʾ�������й������ϲ��ص�˵����ȷ����
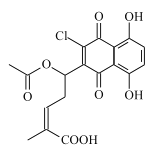
A.�������Ȼ��뱽��һ������ͬһƽ��
B.�����ϲ���������������ˮ��ɻ������
C.�����ϲ��ز�����Na2CO3 ��Һ��Ӧ
D.1 mol �����ϲ�������ˮ��Ӧ�������� 4 mol Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���2molA��2molB���������������ݻ�Ϊ2L��ij�ܱ������У��������·�Ӧ��3A(g)+B(g)![]() xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬����ʱ���D��C��Ũ�Ⱦ�Ϊ0.4mol/L������д���пհף�
xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬����ʱ���D��C��Ũ�Ⱦ�Ϊ0.4mol/L������д���пհף�
(1)xֵ����_____________��
(2)A��ת����Ϊ_______________��
(3)����D�ķ�Ӧ����Ϊ_____________��
(4)�������Ӧ��ϵ��ѹǿ����ƽ����ϵ��C���������� _________������С�䣩��
(5)�ڴ��¶��£��û�ѧ��Ӧ��ƽ�ⳣ��k=__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)���������õ������£�NH4+����������Ӧ��������NO3-��������Ӧ�������仯ʾ��ͼ���£�
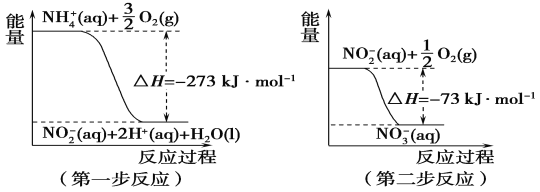
�ٵ�һ����Ӧ��________(��������������������)��Ӧ��
��1 mol NH4+(aq)ȫ��������NO3-(aq)���Ȼ�ѧ����ʽ��__________________��
(2)��298 K��101 kPaʱ����֪��2H2O(g)=O2(g)+2H2(g)����H1��
Cl2(g)+H2(g)=2HCl(g)�� ��H2��
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)����H3��
����H3����H1����H2֮��Ĺ�ϵ��ȷ����___________��
A.��H3=��H1+2��H2 B.��H3=��H1+��H2
C.��H3=��H1-2��H2 D.��H3=��H1-��H2
(3)��֪���ױȰ����ȶ�����ӦP4(���ף�s)+5O2(g)=2P2O5(s)����H1��P(���ף�s)��5O2(g)=2P2O5(s)����H2����H1����H2�Ĺ�ϵ����H1_________��H2(����>������<������=��)��
(4)��֪H2(g)��Br2(l)=2HBr(g)����H=-72 kJ/mol������1 mol Br2(l)��Ҫ���յ�����Ϊ30 kJ����������������±���
���� | H2(g) | Br2(g) | HBr(g) |
1 mol�����еĻ�ѧ������ʱ��Ҫ���յ�����(kJ) | 436 | 200 | a |
�����a=________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�棬101kPaʱ���4.6g�Ҵ�������O2����ȫȼ�գ��ų�136.68kJ���������÷�Ӧ���Ȼ�ѧ����ʽ��ȷ����
A.C2H5OH(l)��2O2(g) = 2CO(g)��3H2O(l) ��H����1366.8 kJmol��1
B.C2H5OH(l)��3O2(g) = 2CO2(g)��3H2O(l)����H����1366.8 kJmol��1
C.C2H5OH(l)��3O2(g) = 2CO2(g)��3H2O(g)����H����136.68 kJmol��1
D.C2H5OH(l)��3O2(g) = 2CO2(g)��3H2O(l)����H��1366.8 kJmol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�ϵ�ı����У���ȷ����
A. 0.1 mol��L��1NaHSO4��Һ�У�c(Na��)��c(H��)��c(SO![]() )��c(OH��)
)��c(OH��)
B. �к�pH���������ͬ������ʹ�����Һ������NaOH�����ʵ���֮��Ϊ1��1
C. 0.1 mol��L��1NaHCO3��Һ�У�c(Na��)>c(HCO![]() )>c(CO
)>c(CO![]() )>c(H2CO3)
)>c(H2CO3)
D. pH��3�������pH��3��AlCl3��Һ�У�ˮ�������c(H��)���ߴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ģ���������������ˮ�Ĺ���ԭ��ʾ��ͼ���¡���֪X��Y��Ϊ���Ե缫��ģ�⺣ˮ�к�Na����Cl����Ca2����Mg2����SO42-�����ӡ�������������ȷ���ǣ� ��
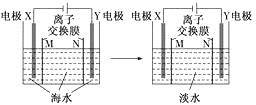
A.N�������ӽ���Ĥ
B.Y�缫�ϲ�����ɫ����
C.X�缫�����л��Dz���
D.X�缫��ӦʽΪ2H2O��4e��=4H����O2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com